第二章化学反应速率和化学平衡第二节影响化学反应速率的因素有利的——越快越好
有利的——越快越好
有害的——越慢越好
有害的——越慢越好
能否控制化学反应速率呢
能否控制化学反应速率呢
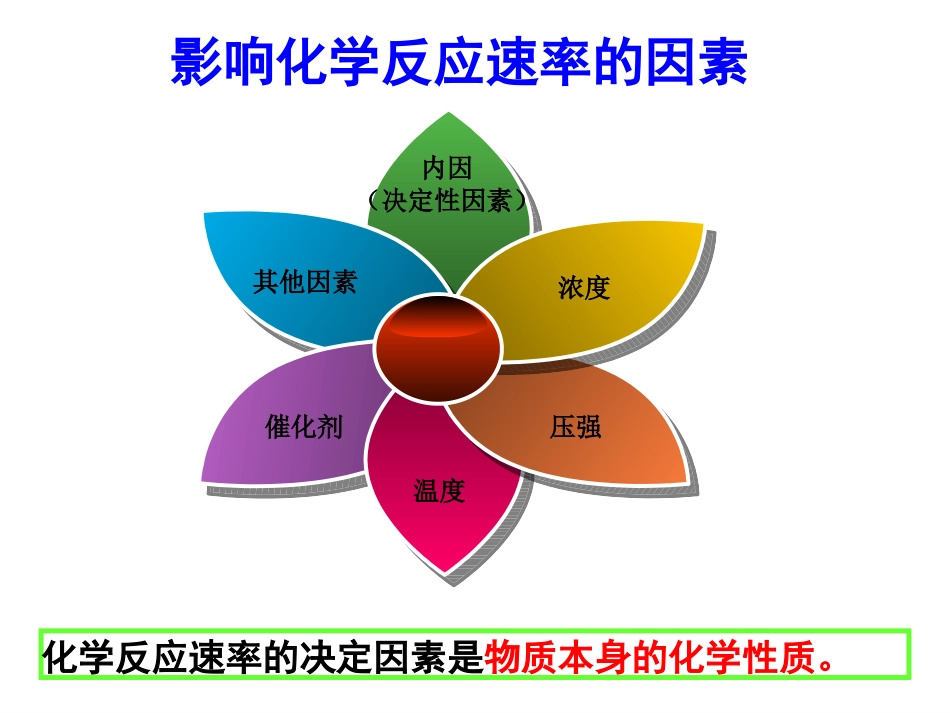
化学反应速率的决定因素是物质本身的化学性质
其他因素内因(决定性因素)浓度催化剂压强温度影响化学反应速率的因素没合适的取向没足够的能量足够的能量+合适的取向投篮化学反应有效碰撞有效碰撞无效碰撞无效碰撞活化分子百分数:(活化分子数/反应物分子数)×100%化学反应速率主要取决于:普通分子活化能活化分子合理取向碰撞有效碰撞新物质单位体积内活化分子数有效碰撞的几率结论:在其他条件不变时,增大反应物浓度,可以增大反应速率现象:H2C2O4溶液浓度大,KMnO4先褪色2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O一、浓度对反应速率的影响探究实验探究实验::0
01mol/L的KMnO4溶液0
1mol/LH2C2O4溶液0
2mol/LH2C2O4溶液快慢本质原因:反应物浓度增大反应速率加快活化分子数增大单位体积内有效碰撞次数增加应用1:一定条件下,在CaCO3(块状)+2HCl=CaCl2+H2O+CO2反应中,为了加快反应的速率,下列那些方法可行()A、增加HCl的浓度B、加水C、增加同浓度盐酸的量D、改加CaCO3粉末AD注意事项:浓度的影响只适用于气体或溶液的反应,固体、纯液体的浓度均可视为常数
固体反应物速率与表面积有关:表面积越大,反应速率越大随着化学反应的进行,反应物的浓度会逐渐减小,因此一般反应速率也会逐渐减小
二、压强对反应速率的影响压强增大气体的体积缩小浓度增大化学反应速率增大化分子数增大单位体积内活二、压强对反应速率的影响压强对反应的影响本质上是浓度的影响增大压强,浓度增大,反应速率加快;减小压强,反应速率减慢
压强只对于有气体参加