高中化学电解池知识点练习题、单选题1
下列叙述中正确的是()①电解池是将化学能转变成电能的装置②原电池是将电能转变成化学能的装置③轮船上嵌入锌块来减缓轮船腐蚀的方法叫牺牲阳极的阴极保护法④不能自发进行的氧化还原反应,通过电解的原理有可能实现⑤电镀过程相当于金属的“迁移”,可视为物理变化⑥锌与稀H2SO4反应时,加入少量CuSO4溶液时,可以加快化学反应速率A.③④⑥B.①③④C.②④⑤D.①②③2
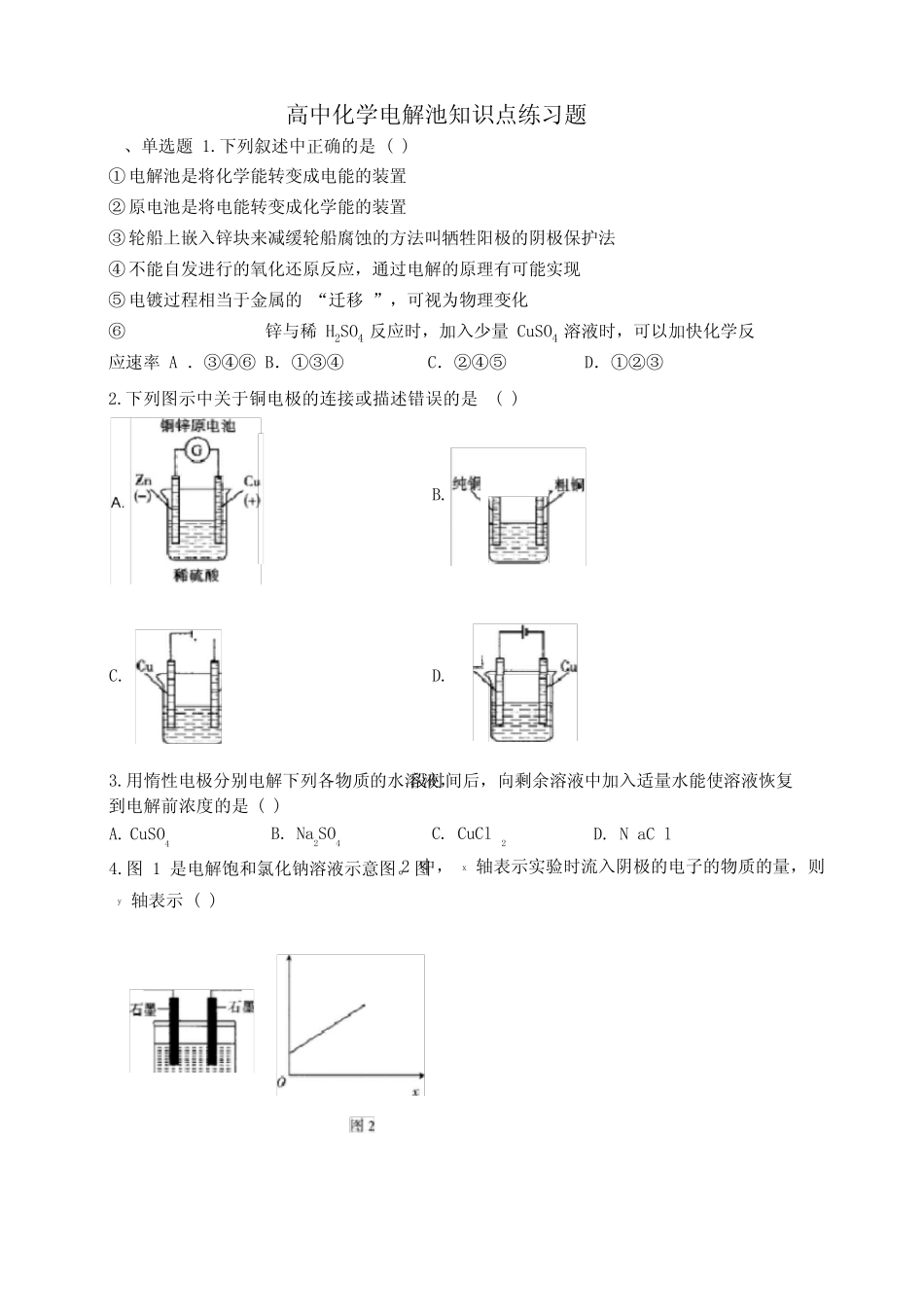
下列图示中关于铜电极的连接或描述错误的是()到电解前浓度的是()C
用惰性电极分别电解下列各物质的水溶液,段时间后,向剩余溶液中加入适量水能使溶液恢复A
CuSO4B
Na2SO4C
CuCl2D
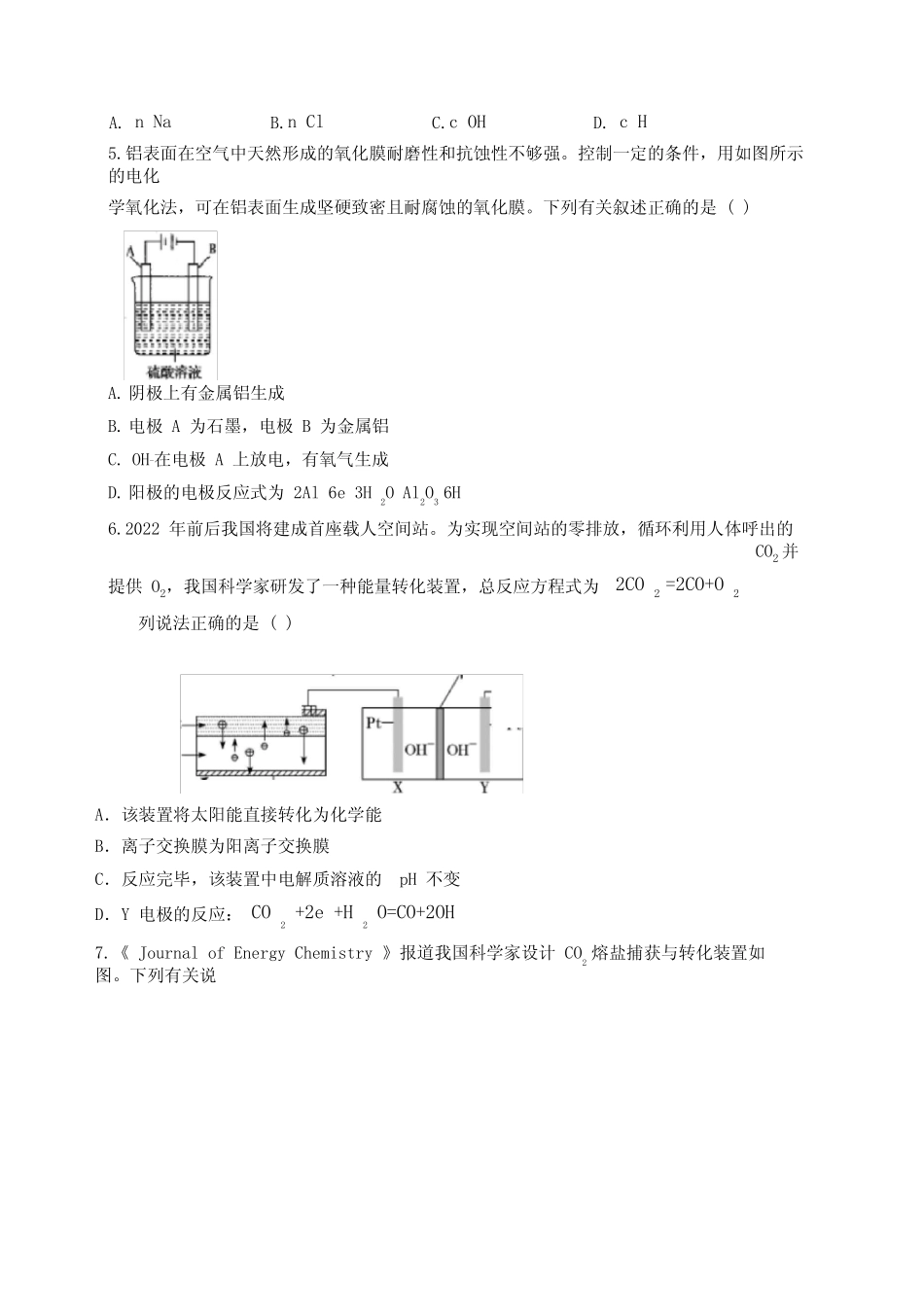
图1是电解饱和氯化钠溶液示意图
图2中,x轴表示实验时流入阴极的电子的物质的量,则y轴表示()B
铝表面在空气中天然形成的氧化膜耐磨性和抗蚀性不够强
控制一定的条件,用如图所示的电化学氧化法,可在铝表面生成坚硬致密且耐腐蚀的氧化膜
下列有关叙述正确的是()A
阴极上有金属铝生成B
电极A为石墨,电极B为金属铝C
OH-在电极A上放电,有氧气生成D
阳极的电极反应式为2Al6e3H2OAl2O36H6
2022年前后我国将建成首座载人空间站
为实现空间站的零排放,循环利用人体呼出的CO2并提供O2,我国科学家研发了一种能量转化装置,总反应方程式为2CO2=2CO+O2列说法正确的是()A.该装置将太阳能直接转化为化学能B.离子交换膜为阳离子交换膜C.反应完毕,该装置中电解质溶液的pH不变D.Y电极的反应:CO2+2e+H2O=CO+2OH7
《JournalofEnergyChemistry》报道我国科学家设计CO2熔盐捕获与转化装置如图
下列有关说A
cH法正确的是()A
熔盐可用KOH溶液代替22C
d的电极反应式为C