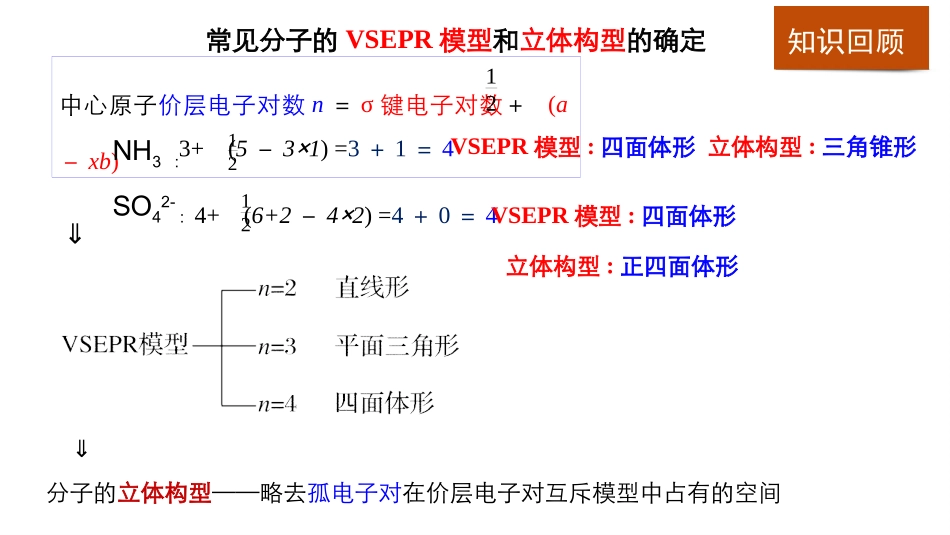
常见分子的VSEPR模型和立体构型的确定中心原子价层电子对数n=σ键电子对数+(a-xb)12知识回顾NH3:4+(6+2-4×2)=4+0=4SO42-:3+(5-3×1)=3+1=41212VSEPR模型:四面体形VSEPR模型:四面体形立体构型:正四面体形立体构型:三角锥形⇓⇓分子的立体构型——略去孤电子对在价层电子对互斥模型中占有的空间1
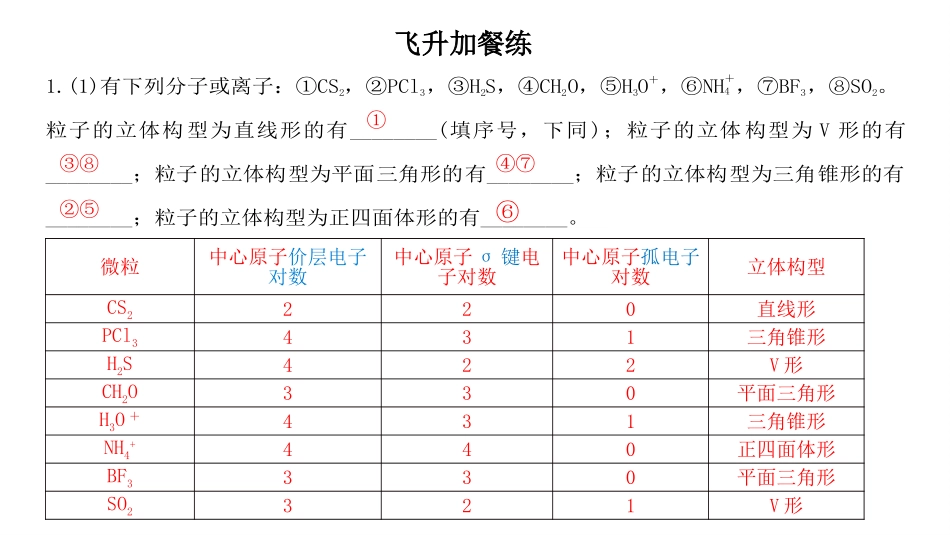
(1)有下列分子或离子:①CS2,②PCl3,③H2S,④CH2O,⑤H3O+,⑥NH+4,⑦BF3,⑧SO2
粒子的立体构型为直线形的有________(填序号,下同);粒子的立体构型为V形的有________;粒子的立体构型为平面三角形的有________;粒子的立体构型为三角锥形的有________;粒子的立体构型为正四面体形的有________
微粒中心原子价层电子对数中心原子σ键电子对数中心原子孤电子对数立体构型CS2220直线形PCl3431三角锥形H2S422V形CH2O330平面三角形H3O+431三角锥形NH4+440正四面体形BF3330平面三角形SO2321V形飞升加餐练①③⑧④⑦②⑤⑥(2)若ABn的中心原子上有一对孤电子对未能成键,当n=2时,其立体构型为________;当n=3时,其立体构型为________
12(a-xb)=1σ=2V形三角锥形σ=3C==O键与C—Cl键之间电子对的排斥作用强于C—Cl键与C—Cl键之间电子对的排斥作用(3)俗称光气的氯代甲酰氯分子(COCl2)为平面三角形,但C—Cl键与C==O键之间的夹角为124
3°;C—Cl键与C—Cl键之间的夹角为111
4°,解释其原因:分子中价层电子对之间的斥力主要顺序为:ⅰ
孤电子对之间的斥力>孤电子对与共用电子对之间的斥力>共用电子对之间的斥力;ⅱ
双键与双键之间的斥力>双键与单键之间的斥力>单键与单键之间的斥力;ⅲ