课题3二氧化碳和一氧化碳贵州省德江县桶井中学姜春玉请选择出实验室正确制取CO2的装置回顾:ABCDCO2CO2CO2可见:二氧化碳的密度为比空气大
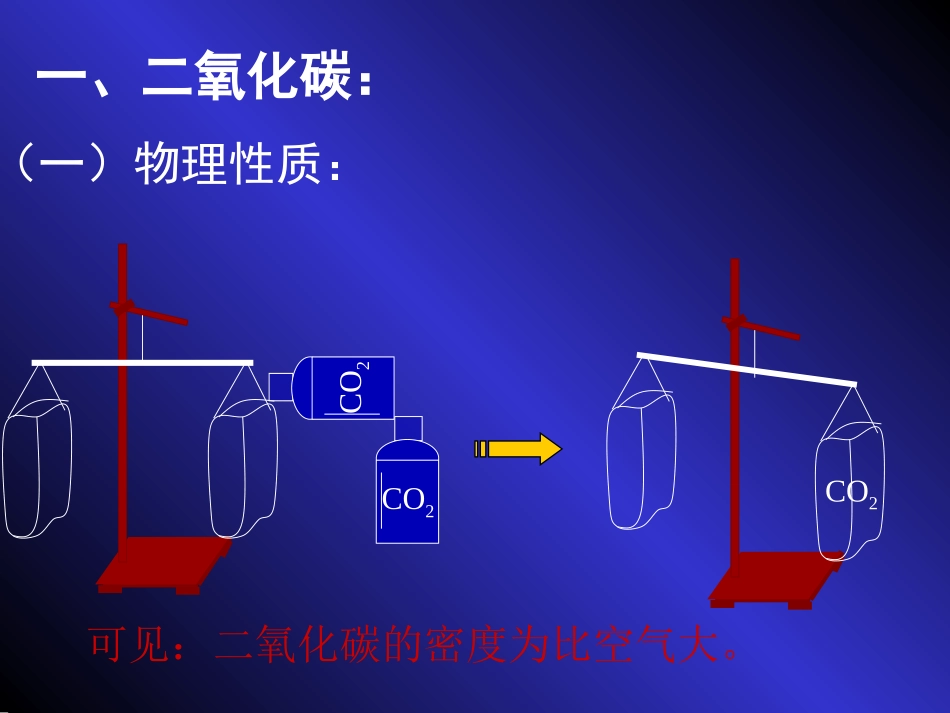
一、二氧化碳:(一)物理性质:在通常情况下,二氧化碳是无色无味气体;在标况下,二氧化碳的密度为1
977g/L,比空气大;能溶于水
二氧化碳的固体俗称干冰
结论:(二)化学性质:1、不能供给呼吸;2、既不能燃烧,也不能支持燃烧;(通常情况下)石蕊试液3、二氧化碳与水反应:稀醋酸稀盐酸A石蕊和某些酸的反应B直接放入CO2中C喷水D喷水后放入CO2中探究什么物质使紫色石蕊试液变红色:二氧化碳与水反应原理:CO2+H2O===H2CO3H2CO3===CO2↑+H2O现象:通入二氧化碳时,紫色石蕊试液变红色
碳酸不稳定,加热易分解
当加热上述变红色的溶液,二氧化碳气体逸出,红色又变成紫色
4、与石灰水反应:现象:澄清的石灰水变浑浊
原理:CO2+Ca(OH)2=CaCO3↓+H2O碳酸钙此反应原理是用来检验或鉴定二氧化碳气体
讨论:为了使用石灰浆[Ca(OH)2]抹的墙壁快点干燥,为什么常常需在室内生炭火盆
为什么开始放炭火盆时,墙壁反而潮湿
CO2+Ca(OH)2=CaCO3↓+H2O碳酸钙5、二氧化碳与还原性金属或非金属单质反应:(1)二氧化碳与镁带的反应:现象:将燃着的镁带伸进盛有二氧化碳的集气瓶中,镁带继续燃烧,瓶壁上有黑色物质生成,瓶底有白色固体物质出现
原理:CO2+2Mg==2MgO+C点燃(2)二氧化碳与碳的反应:原理:CO2+C==2CO高温注意:(1)燃烧不一定需要氧气参加;(3)上述两反应中二氧化碳是氧化剂,镁、碳是还原剂
(2)二氧化碳在特殊条件下也能支持燃烧
(三)二氧化碳的用途:1、灭火;灭火的原因是:二氧化碳既不能燃,也不支持燃,且密度比空气大,所以,二氧化碳能覆盖在可燃物的表面,使可燃物隔绝氧气而熄灭