智慧的火花智慧的火花想想看:想想看:你如何得知一粒大米的质量
对于微小的物质,扩大倍数形成一定数目的集体,可以使研究更方便
[问题一]下列化学方程式所表达的意义是什么
[问题二]在实验室里拿2个氢气分子与1个氧气分子反应容易做到吗
2H2+O2==2H2O点燃表示反应物与生成物氢气氧气水分子数之比2个1个2个质量之比4g32g36g扩大6
02×1023倍2×6
02×10236
02×10232×6
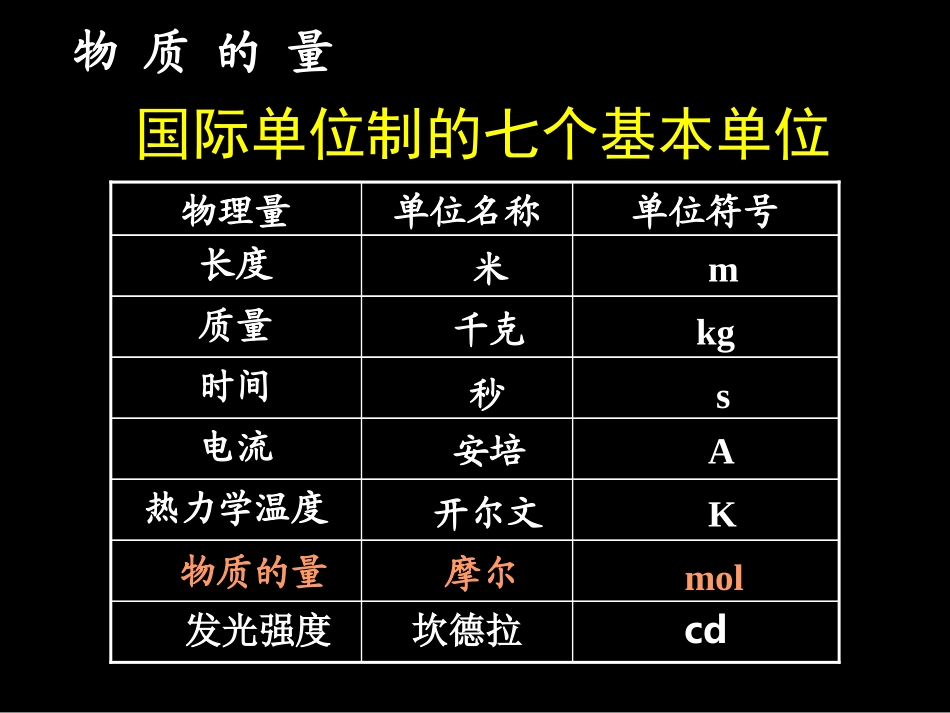
02×1023物质的量2mol1mol2mol物质的量国际单位制的七个基本单位国际单位制的七个基本单位cd坎德拉发光强度热力学温度电流时间质量长度单位符号单位名称物理量米安培A开尔文K摩尔mol千克秒mkgs物质的量物质的量是国际单位制七个基本物理量之一表示含有一定数目微观粒子的集体符号:n分子、原子、离子、质子、电子……物质的量“物质的量”是一个整体,不可拆开物质的量的单位是摩尔物质的量符号:mol1打毛巾1打作业本1打袜子12条12本12双宏观物质摩尔微观粒微观粒子子1molmol分子离子原子……
个NNAA个1令白纸500物质的量阿伏加德罗常数(NA)NA=0
012kg12C所含的碳原子数≈6
02×1023mol-1注意:不能认为6
02×1023就是阿伏加德罗常数物质的量阿伏加德罗常数符号:定义值:0
012kgC-12所含的C原子数含义:1mol任何粒子所含的粒子数均为阿伏加德罗常数个近似数值:约为6
02×1023单位:mol—112克NA物质的量注注意意使用时必须指明是哪一种粒子仅用于计量微观粒子1mol大米()×1mol氢()×1molCO2()√1
1molH2所含氢气分子的个数
2mol氢分子含个氢原子
1molSO42-含个硫酸根离子
204×1024个H2含多少mol氢气分子
5mol的O2中有多少个氧