课题2二氧化碳制取的研究我们已经学过碳在氧气中燃烧、高温下碳还原氧化铜都可以生成二氧化碳,那么在实验室里能否用这些方法来制备二氧化碳呢
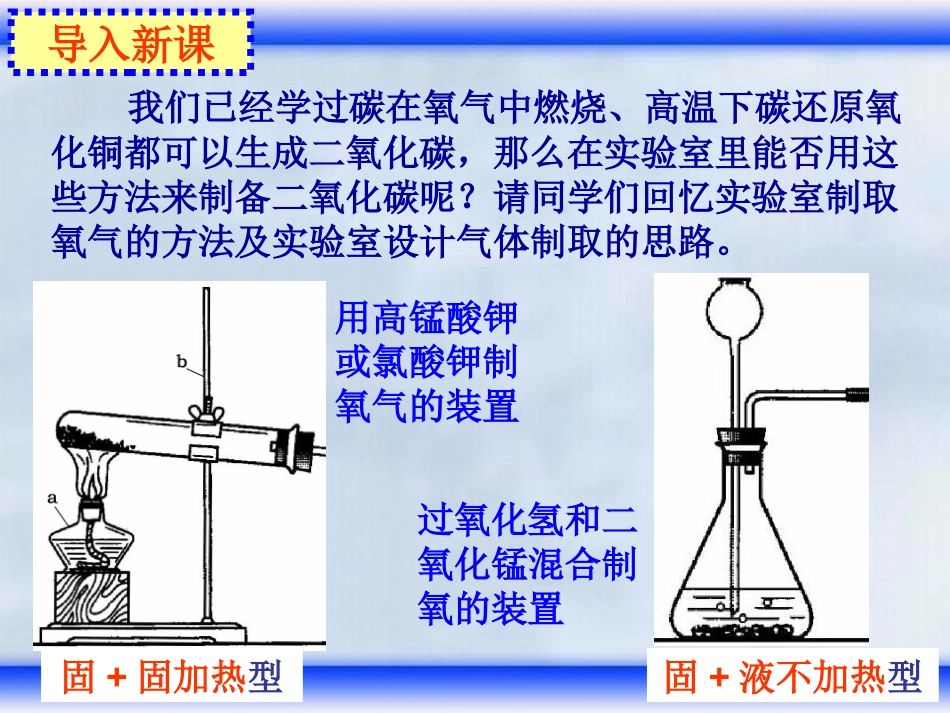
请同学们回忆实验室制取氧气的方法及实验室设计气体制取的思路
过氧化氢和二氧化锰混合制氧的装置导入新课固+固加热型固+液不加热型用高锰酸钾或氯酸钾制氧气的装置•[实验探究]•探究实验室制取二氧化碳的理想原料:•可供选择的药品:⑴碳酸钠粉末(Na2CO3);⑵石灰石或大理石(CaCO3);⑶稀盐酸(HCl);⑷稀硫酸(H2SO4)
•可供选择的仪器:试管、药匙、胶头滴管
•方法:将药品⑴⑵分别与药品⑶⑷两两反应,观察反应速度快慢
一、实验室制取CO2的反应原理推进新课碳酸钠和稀盐酸、稀硫酸反应速度太快;石灰石(或大理石)和稀硫酸反应一会便自动停止;石灰石(或大理石)和稀盐酸反应速度适宜、平稳
药品:大理石(或石灰石)和稀盐酸2
反应原理:CaCOCaCO33++2HCl2HCl==CaClCaCl22++HH22OO++COCO22↑↑实验结果CaCO3+H2SO4=CaSO4+H2O+CO2↑生成了微溶物硫酸钙,覆盖在石灰石表面,阻碍反应继续进行
因为浓盐酸易挥发出HCl气体,导致收集的二氧化碳不纯
因为碳酸钠和稀盐酸反应速度太快、不易控制
(1)为什么不能用稀硫酸代替稀盐酸
(2)为什么不能用碳酸钠
(3)为什么不能用浓盐酸
请同学们根据上图和课本113页回答:1
实验室制取气体的装置由哪几部分组成
确定气体发生装置时应考虑哪些因素
确定气体收集装置时应考虑哪些因素
二、实验室制取二氧化碳的装置[归纳]实验室里制取气体的装置的确定方法实验室制取气体的装置气体发生装置反应物的状态反应条件(是否需要加热等)固体和固体反应固体和液体反应液体和液体反应排空气法排水法(不易溶于水、不与水发生反应)密度大于空气——向上排气法密度小于空