第二节离子反应第1课时酸、碱、盐在水溶液中的电离1
了解电解质与非电解质的概念2
理解电离的定义3
能用电离方程式表达常见、典型的电解质在水溶液中的电离
从电离的角度认识酸、碱、盐
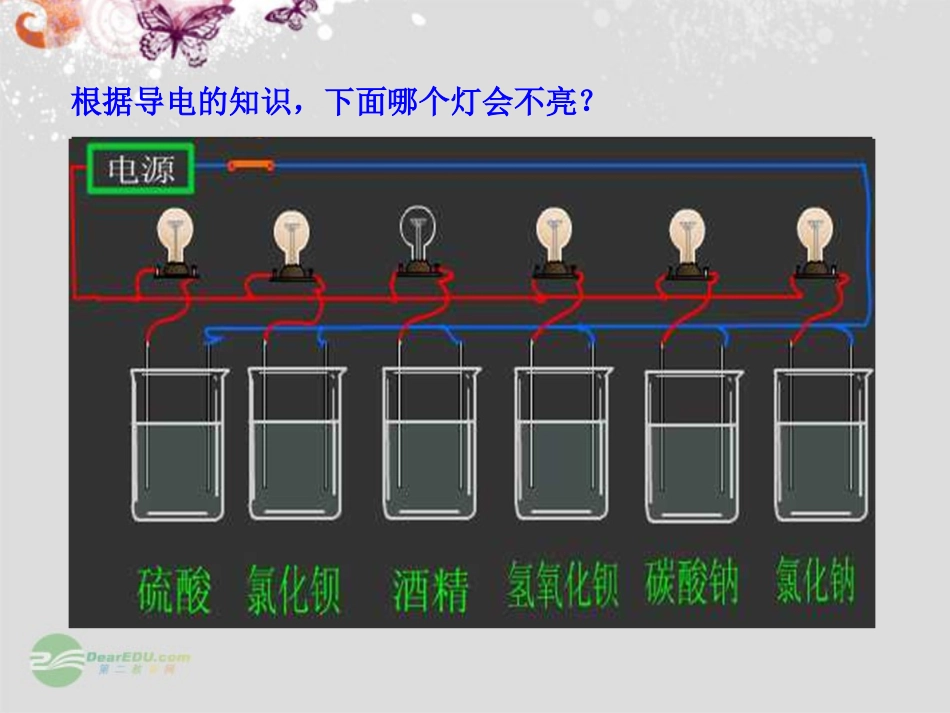
根据导电的知识,下面哪个灯会不亮
熔融的硝酸钾也能导电概念:在水溶液中或熔融状态下能够导电的化合物例如:KNO3、NaOH、H3PO4等,都是电解质
酸、碱、盐、部分金属氧化物和水是电解质利用树状分类法分析一、电解质非电解质:在水溶液中或熔融状态下不能够导电的化合物化合物电解质:在水溶液中或熔融状态下能够导电的化合物非金属氧化物、大部分有机物是非电解质物质混合物纯净物化合物单质电解质:非电解质:乙醇、蔗糖等大部分有机物不是电解质,也不是非电解质对电解质的理解酸、碱、盐、水、活泼金属氧化物带正电荷的阳离子和带负电荷的阴离子金属导电自由移动电子溶液导电自由移动电荷自由移动电荷金属和溶液能够导电的原因是什么
酸、碱、盐溶液导电是它们在溶液中发生了电离氯化钠在水中电离NaCl在水中的溶解和电离的示意图二、电离1、定义:电解质在水溶液中或熔融状态下产生能够自由移动的离子的过程2、电离的表示——电离方程式用化学符号表示电解质电离成自由移动离子的过程
如:NaCl=Na++Cl-现在你明白电解质溶液能导电和非电解质不能导电的原因了吗
电解质和非电解质在水中电离的比较问题探究1SO2属于化合物,溶于水也导电,SO2属于电解质吗
电解质是指在水溶液里或熔融状态下能自身电离而导电的化合物
SO2溶于水导电是因为生成H2SO3,电离产生自由移动的离子而导电,应该理解为H2SO3是电解质,SO2属于非电解质
分析电离方程式NaCl====Na++Cl-阳离子阴离子化学式生成符号离子符号(代表水合离子)问题探究2如何正确的书写电离方程式
Al2(SO4)3=2Al3++3SO42-2
书写步骤:(1)阴阳离子部分