第二章化学物质及其变化第3节氧化还原反应得到氧,被氧化(氧化反应)△CuO+H2==Cu+H2O失去氧,被还原(还原反应)CuOHHCuHHO从得氧失氧角度分析:氧化还原反应:一种物质被氧化(得到氧),同时一种物质被还原(失去氧)的反应
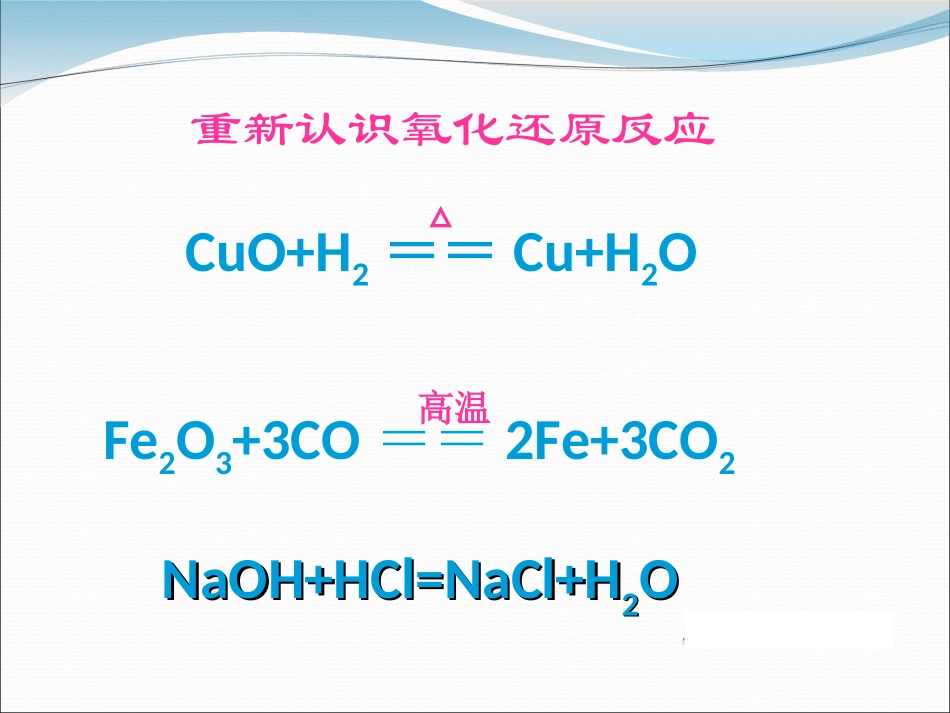
CuO+H2==Cu+H2O重新认识氧化还原反应Fe2O3+3CO==2Fe+3CO2△高温NaOH+HCl=NaCl+HNaOH+HCl=NaCl+H22OOFe2O3+3CO=2Fe+3CO2被还原,发生还原反应被氧化,发生氧化反应氧化还原反应:一种物质被氧化同时一种物质被还原的反应
CuO+H2=Cu+H2O被还原,发生还原反应被氧化,发生氧化反应+3+20+4+200+1化合价降低化合价升高化合价降低化合价升高化合价降低化合价升高一、从化合价升降观点的认识反应还原剂氧化剂2Na+Cl2==2NaCl00+1-1失电子,化合价升高,被氧化得电子,化合价降低,被还原离子化合物NaCl的形成过程化合价升降的原因:电子的得失NaCl失去e-失去e-后得到e-后Na+[Cl]-Cl-Na+三、氧化还原反应的实质:H2+Cl2===2HCl00+1-1电子对偏离,化合价升高,被氧化电子对偏向,化合价降低,被还原[结论]氧化还原反应的实质是:发生了电子的转移(得失或偏移)共价化合物HCl的形成过程化合价升降的原因:电子的偏移HClHCl元素化合价和电子得失的关系化合价升高,被氧化化合价降低,被还原2Na+Cl2=2NaCl00+1-1NaNa+ClCl-Cl-Na+电子转移元素化合价数离子化合物:=该元素一个原子得失电子数化合价升高数=失去的电子数化合价降低数=得到的电子数失去电子的反应就是氧化反应得到电子的反应就是还原反应化合价升降观点电子转移观点氧化反应还原反应氧化还原的关系氧化还原反应化合价升高的反应化合价降低的反应化合价升高降低同时发生有