四川宜宾四川阆中第3节分子的性质zxxkw学
网1、写出H2、F2、N2、HCl、CO2、H2O的电子式和结构式
2、以上分子中的共用电子对是否会发生偏移
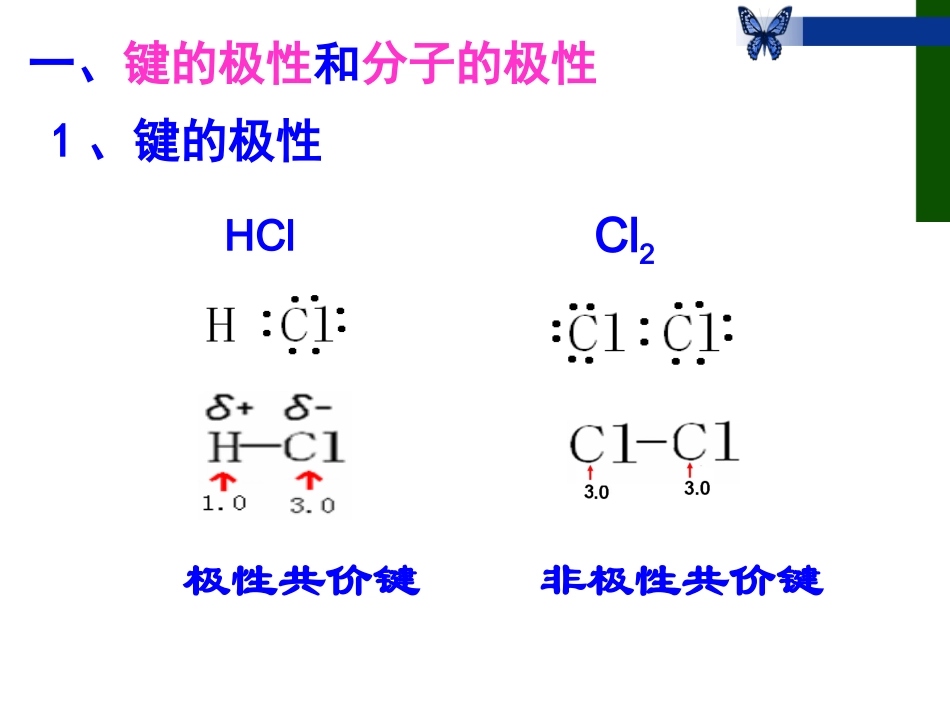
电子式结构式电子式结构式F:F::::::F-FH:O:H::H-O-H知识回顾极性共价键非极性共价键一、键的极性和分子的极性1、键的极性HClCl21、键的极性的本质是什么
共用电子对是否偏移思考与交流2、共用电子对发生偏移的原因是什么
成键原子对共用电子对的吸引能力(电负性)3、键的极性的判断依据是什么
(1)成键元素的电负性比较(2)成键原子是否属于同种元素zxxkw非极性键:同种元素的原子间形成的共价键
极性键:不同种元素的原子间形成的共价键
1、指出下列物质中化学键的类型
若是共价键,请判断键的极性:(1)F2(2)HF(3)NaOH(4)N2(5)Na2O2(6)H2O2(7)CsCl(8)CH3COOH2、含有非极性键的离子化合物是:A
Na2O2C
NH4Cl知识回顾3、下列元素间形成的共价键中,极性最强的是:A
网一、键的极性和分子的极性2、分子的极性(1)定义:极性分子:分子的正电中心与负电中心不重合的共价分子
非极性分子:分子的正电中心与负电中心重合的共价分子
(2)判定方法:类型1:单质分子一般属非极性分子①单原子分子:HeNeArKrXeRn②双原子分子:③多原子分子:H—HCl—Clzxxkw(2)判定方法:类型2:共价化合物分子属极性分子H—ClCO①双原子化合物:(2)判定方法:CO2CH4H2OCH2O②单中心多原子化合物:BF3NH3思考:以下分子是极性还是非极性
(2)判定方法:分子中心原子价层电子对数有无孤电子对所连原子是否相同分子极性CO2C2无相同BF3B3无相同CH4C4无相同H2OO4有相同NH3N4