第1课时原子核外电子的排布及元素周期律学习目标1
了解原子核外电子排布
掌握元素核外电子、化合价、原子半径周期性变化规律
学习过程一、核外电子排布1
核外电子运动特征根据所给的一些数据请你总结电子运动的特征
(1)核外电子的质量:9
10×10-31kg
(2)炮弹的速度2km/s,人造卫星7
8km/s,宇宙飞船11km/s,氢核外电子2
2×108m/s
(3)乒乓球半径:4×10-2m;原子半径:约10-10m
核外电子分层排布阅读课本P13~14完成下表电子层序号1234567电子层符号电子能量电子离核由到,电子能量由到3
核外电子排布的规律阅读课本P13~14表12,及下表数据,归纳总结核外电子排布的规律
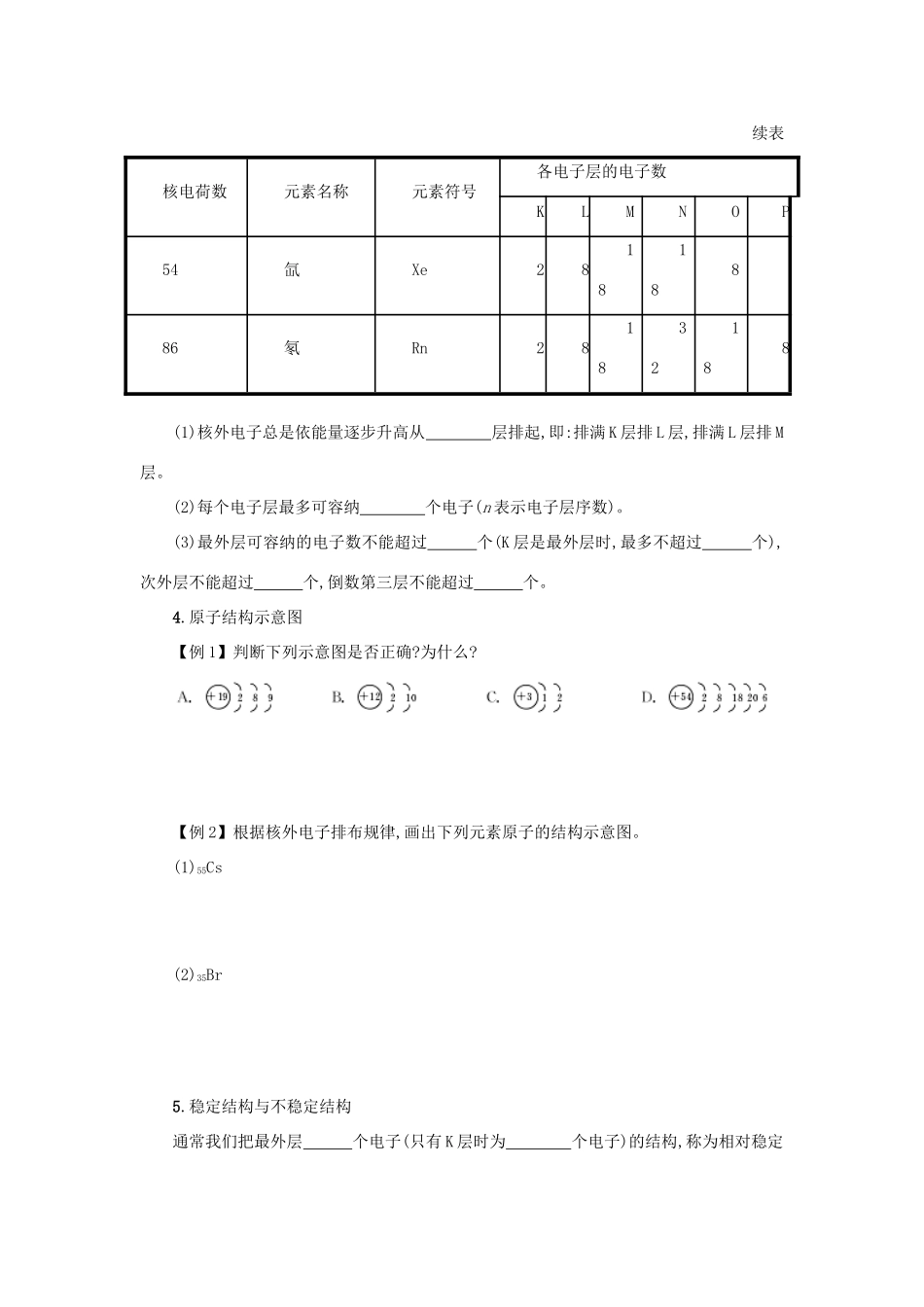
核电荷数元素名称元素符号各电子层的电子数KLMNOP2氦He210氖Ne2818氩Ar28836氪Kr28188续表核电荷数元素名称元素符号各电子层的电子数KLMNOP54氙Xe281818886氡Rn281832188(1)核外电子总是依能量逐步升高从层排起,即:排满K层排L层,排满L层排M层
(2)每个电子层最多可容纳个电子(n表示电子层序数)
(3)最外层可容纳的电子数不能超过个(K层是最外层时,最多不超过个),次外层不能超过个,倒数第三层不能超过个
原子结构示意图【例1】判断下列示意图是否正确
【例2】根据核外电子排布规律,画出下列元素原子的结构示意图
(1)55Cs(2)35Br5
稳定结构与不稳定结构通常我们把最外层个电子(只有K层时为个电子)的结构,称为相对稳定结构
化学反应中,具有不稳定结构的原子,总是“想方设法”通过各种方式使自己的结构趋向于稳定
二、元素周期律1
电子层排列的周期性根据1~18号元素核外电子排布,总结核外电子排布的规律
化合价的周期性变化根据1~18号元素的化合价,总结化合价的变化规律:
(1)1~18