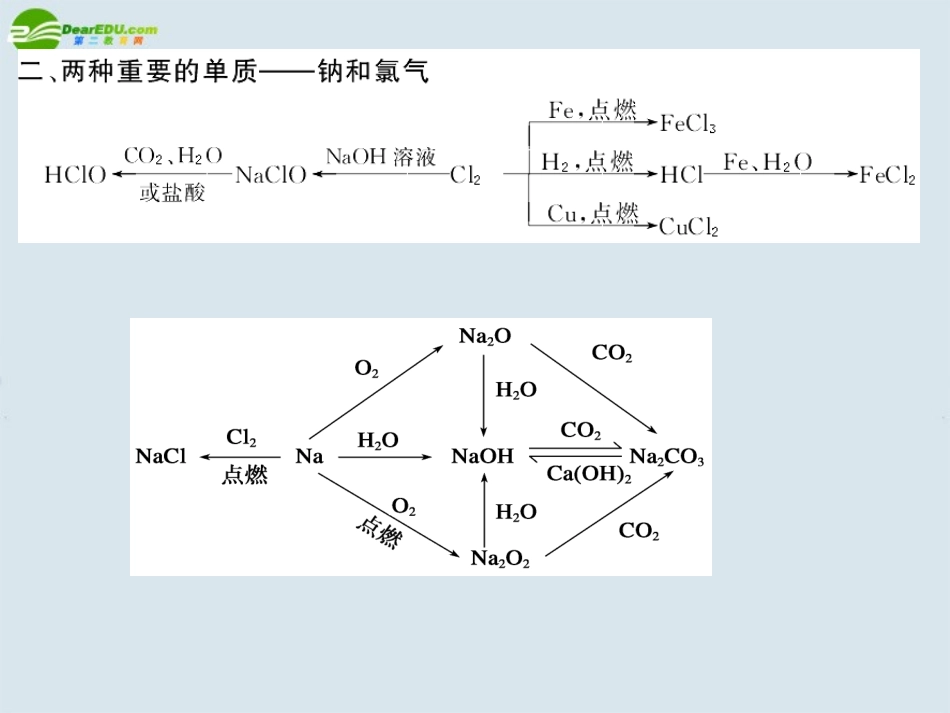
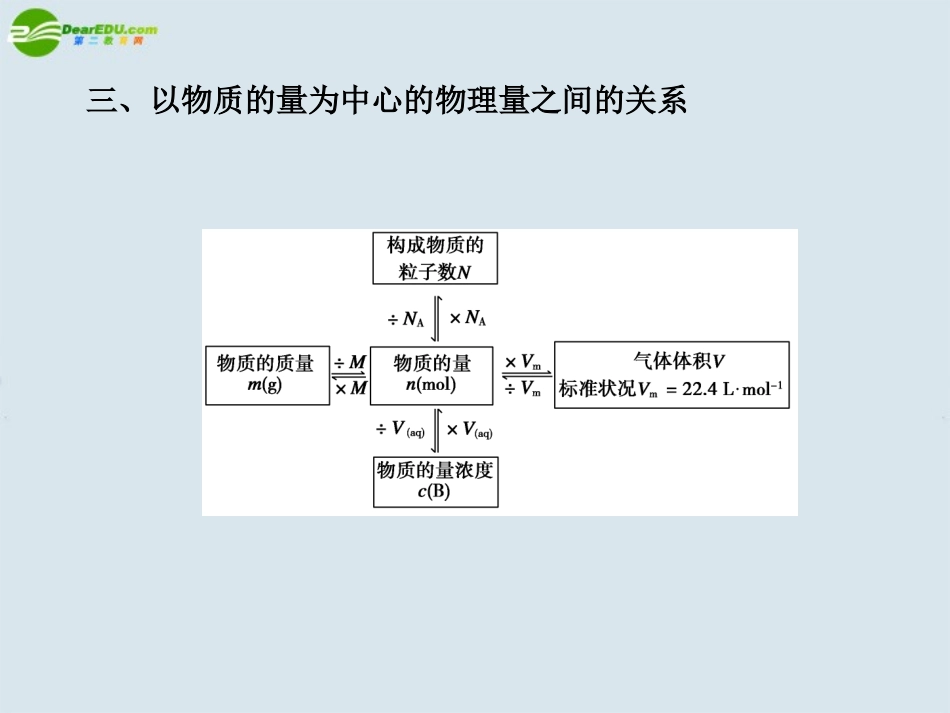
章末总结知识网络三、以物质的量为中心的物理量之间的关系技能提升一、以阿伏加德罗常数为核心的相关计算1.若题目中给出物质的体积一要看是否处于标准状况,若不是标准状况,则1mol气体体积一般不为22
4L;二要看该物质在标准状况下是否为气体,若不是气体,则无法求算该物质的物质的量或分子数目,若是气体,则可用n=V22
4L·mol-1或N=V·NA22
4L·mol-1求算出该物质的n或N,这与是混合气体还是单一气体无关
2.若题目中给出气体物质的质量或物质的量该物质的粒子数目与外界条件(是否处于标准状况下)无关
3.若题目要求计算物质分子中的原子个数需注意物质的组成
例如稀有气体为单原子分子,臭氧(O3)为三原子分子,甲烷(CH4)为五原子分子等
4.若题目要求计算分子、原子、离子中的质子或电子数目需正确运用原子中质子数等于电子数、离子中质子数、电子数、电荷数之间的关系进行求解
【例1】用NA代表阿伏加德罗常数,下列说法正确的是()A.标准状况下,33
6LH2O中含有1
5NA个H2O分子B.常温常压下,2gH2中含有NA个H原子C.标准状况下,22
4L任意比的H2和O2的混合气体中含有的分子总数为NAD.2
4g金属镁变成镁离子时失去的电子数目为0
1NAC二、溶液等体积或等质量混合时质量分数的变化规律1.浓度与密度的变化关系(1)若溶液的密度大于1g·cm-3,则溶质的质量分数越大,其密度就越大
常见溶液有NaCl溶液、稀硫酸等
(2)若溶液的密度小于1g·cm-3,则溶质的质量分数越大,其密度就越小
常见溶液有氨水、酒精等
2.溶液等质量混合时质量分数的变化规律无论溶液的密度大于1g·cm-3,还是小于1g·cm-3,等质量混合时,得混合溶液的质量分数都等于它们和的一半
3.溶液等体积混合时质量分数的变化规律两种不同质量分数的溶液等体积相混合,若溶液的密度大于1g·