第二节硫酸和硝酸的氧化性思考与交流(1)硫酸、硝酸、盐酸都是酸,他们在组成上有什么特点
(2)这种特点与酸的通性有什么关系
用离子方程式表示
(3)实验室里用金属与酸反应制取氢气时,往往用稀硫酸或盐酸,而不用浓硫酸或硝酸,这是为什么
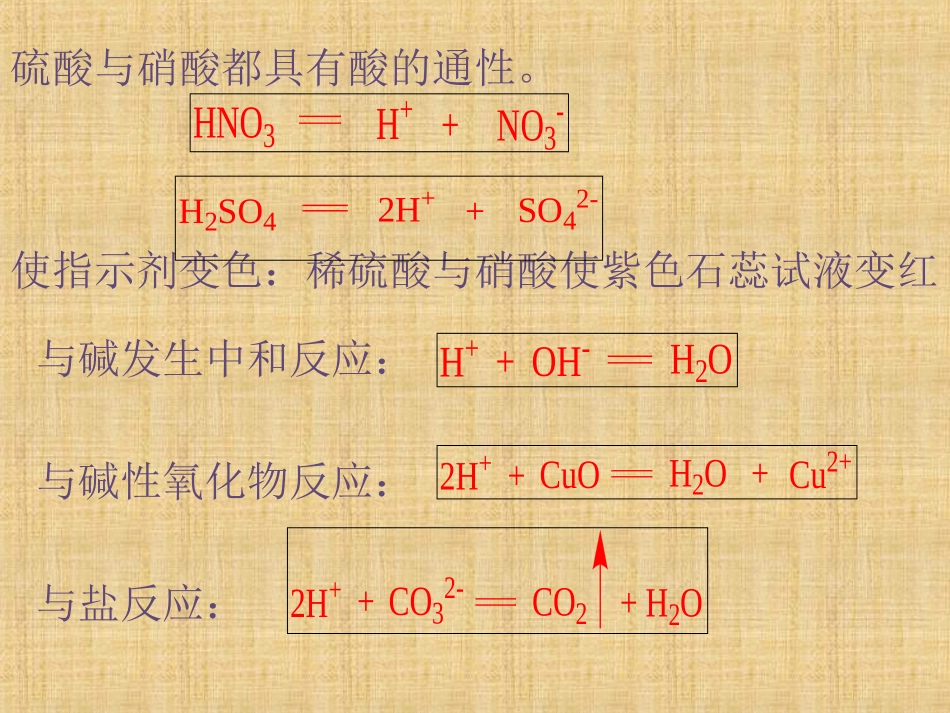
硫酸与硝酸都具有酸的通性
使指示剂变色:稀硫酸与硝酸使紫色石蕊试液变红与碱发生中和反应:与碱性氧化物反应:与盐反应:H2SO4+2H+SO42-HNO3+H+NO3-+H+OH-H2O+2H+H2OCuOCu2+++2H+H2OCO32-CO2+一、浓硫酸1
浓硫酸的物理性质色态:无色、粘稠的油状液体;沸点:约338℃,难挥发性酸(高沸点酸);密度:1
84g/cm3,高密度酸;溶解性:跟水任意比互溶,溶解放出大量热
【思考】浓硫酸应如何稀释
浓硫酸的强氧化性(1)脱水性a
浓硫酸与木屑、棉花、纸屑反应b
浓硫酸与蔗糖反应(2)吸水性【思考】浓硫酸的吸水性与脱水性有什么区别
答:吸水性是指浓硫酸直接与水分子结合
脱水性是指浓硫酸将许多有机物中的氢、氧元素按水分子的比例脱去
与铜反应若铜过量,硫酸能否完全反应
Cu+2H2SO4(浓)CuSO4SO22H2O△++在常温下,浓硫酸跟某些金属,如铁、铝等接触时
能够使金属表面生成一薄层致密的氧化物薄膜,从而阻止内部的金属继续跟硫酸发生反应(钝化现象)
因此,冷的浓硫酸可以用铁或铝的容器贮存
但受热时,浓硫酸可以与铁、铝发生反应
小常识探究:浓硫酸与炭反应是否生成了二氧化碳、水和二氧化硫
按正确的顺序连接下列仪器,并说明你的理由
与木炭反应2H2SO4(浓)2SO2CO22H2O+++C△稀硫酸浓硫酸由电离出的H+引起的,可氧化金属活动顺序表氢前的金属由硫酸分子中+6价硫元素引起的,可氧化金属活动顺序表氢后的金属具有弱氧化性具有强氧化性
能氧化大多数的金属(除Au、Pt)学会对比稀