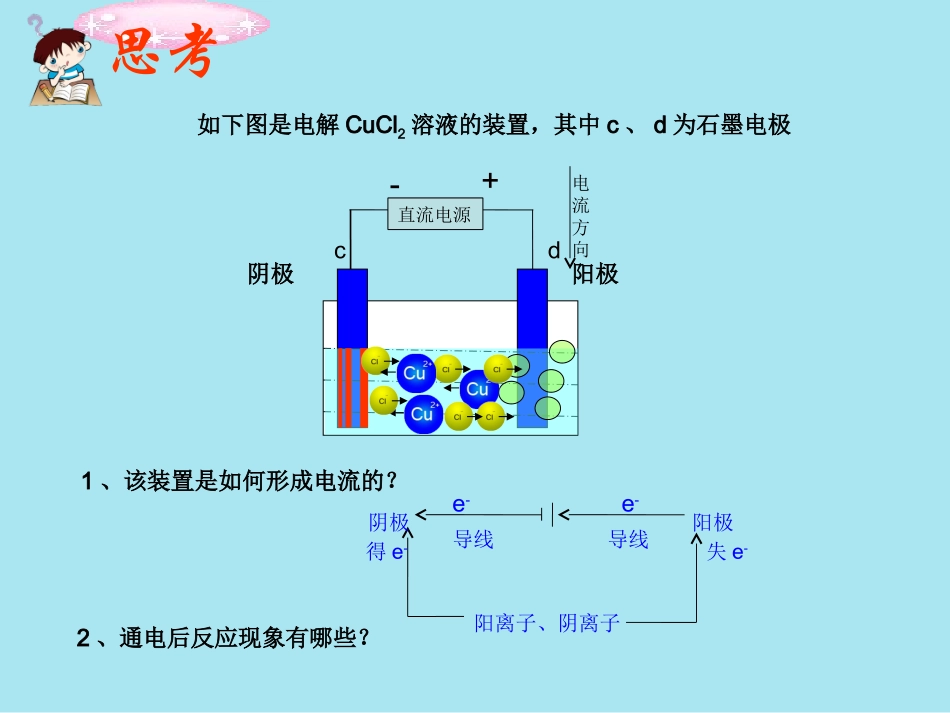
高三化学第一轮复习浠水理工中专杨金容张强婧电解池(第一课时)考纲要求1、了解电解池的工作原理2、了解常见离子在阴阳两极上的放电顺序,能够正确书写电极反应式及总反应方程式3、知道电解在氯碱工业、电镀、电冶金等方面的应用如下图是电解CuCl2溶液的装置,其中c、d为石墨电极阴极阳极直流电源电流方向cd思考2、通电后反应现象有哪些
1、该装置是如何形成电流的
阳离子、阴离子阴极阳极导线导线e-e-得e-失e-+-一、电解原理1.电解定义在直流电作用下,电解质在两个电极上分别发生___________和的过程.2.能量转化形式能转化为能.3.电解池(1)构成条件①有与相连的两个电极.②电解质溶液(或熔融电解质)③形成.(2)反应类型:_________________________氧化反应还原反应电化学直流电源闭合回路非自发的氧化还原反应基础知识梳理【考点释例】用惰性电极电解物质的量浓度相同、体积比为1:3的CuSO4和NaCl的混合溶液
(1)请分别写出阴阳离子放电顺序;(2)依据物质的量和放电顺序,试分析电解过程;(3)试写出电解过程中有关电极反应式和电解总反应式
第一阶段:阳极:2Cl--2e-=====Cl2↑阴极:Cu2++2e-=====Cu2mol2mol1mol2mol总反应式:Cu2++2Cl-=====电解Cu+Cl2↑【知识延伸】常见离子放电顺序:(1)阳极:活性金属做阳极>S2->I->Br->Cl->OH->含氧酸根(2)阴极:Ag+>Fe3+>Cu2+>H+>Pb2+>Sn2+>Fe2+>Zn2+>(H+)第二阶段:阳极:2Cl--2e-=====Cl2↑阴极:2H++2e-=====H2↑1mol1mol1mol1mol总反应式:2Cl-+2H2O=====电解Cl2↑+H2↑+2OH-第三阶段:阳极:4OH--4e-=====2H2O+O2↑;阴极