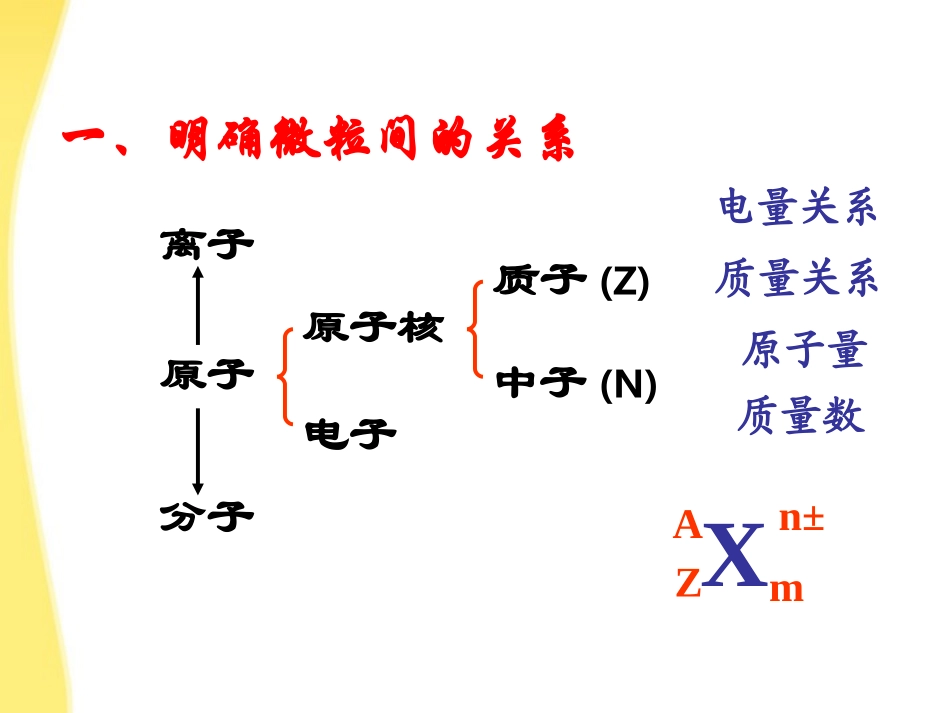
复习第一教时学习目的:1、掌握物质结构的有关概念2、掌握原子结构与元素性质的关系原子分子原子核电子质子(Z)中子(N)离子一、明确微粒间的关系电量关系质量关系质量数原子量XZAmn±例1(00)136C—NMR(核磁共振)可以用于含碳化合物的结构分析,136C表示的碳原子A
核外有13个电子,其中6个能参与成键B
核内有6个质子,核外有7个电子C
质量数为13,原子序数为6,核内有7个质子D
质量数为13,原子序数为6,核内有7个中子D巩固练习例2(97)X、Y、Z和R分别代表四种元素,如果aXm+、bYn+、cZn-、dRm-四种离子的电子层结构相同,则下列关系正确的是A
a-c=m-nB
a-b=n-mC
c-d=m+nD
b-d=n+mD二、核外电子排布的一般规律:1、K层为最外层时,最多容纳电子数------------
2、其他各层为最外层最多容纳电子数------------
3、次外层最多容纳电子数--------------------------
4、倒数第三层最多容纳电子数-------------------
5、第n层最多容纳电子数-------------------------
2个8个18个32个2n2个三、比较微粒的半径大小1、同周期元素的原子或离子2、同主族元素的原子或离子3、相同电子层结构的离子4、同一元素的原子与离子Na、Mg、AlCl-、S2-、P3-F-、Cl-、Br-、I-Li、Na、K、RbO2-、F-、Na+、Mg2+、Al3+Cl、Cl-、Mg2+、Mg、例3(99s)下列化合物中阳离子与阴离子半径比最小的是A
KBrB巩固练习四、理清几个概念的区别与联系1、核数、同位素与同素异形体(1)、4019K和4020Ca(2)、3517Cl和3717Cl(3)、H2和D2(4)、O2和O3(5)、