弱电解质的电离向两支分别盛有0
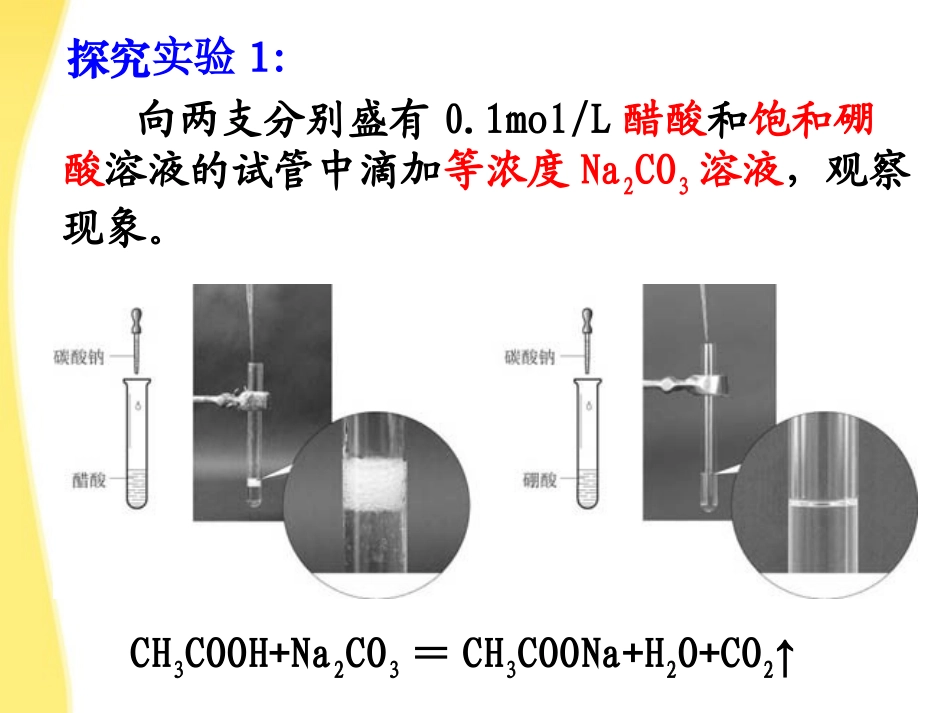
1mol/L醋酸和饱和硼酸溶液的试管中滴加等浓度Na2CO3溶液,观察现象
探究实验1:CH3COOH+Na2CO3=CH3COONa+H2O+CO2↑第一节弱电解质的电离第一节弱电解质的电离第三章水溶液中的离子平衡探究实验2:分别取约2mL浓度均为0
1mol/L的盐酸、醋酸溶液倒入两支试管中,然后分别测定这两种酸的pH
注:测定溶液pH的方法为取一小块试纸在表面皿上,用洁净的玻璃棒蘸取待测液点(或滴)于试纸的中部,观察变化稳定后的颜色,与标准比色卡对照,读出溶液的pH(读数为整数)
结论:HCl完全电离,电离程度为100%
醋酸部分电离,电离程度较小
探究实验2:分别测定0
1mol/L的盐酸、醋酸溶液的pH
1mol/L盐酸0
1mol/L醋酸溶液130
001C(H+)/(mol/L)强电解质:在水溶液中能完全电离的电解质称强电解质
一、强弱电解质一、强弱电解质在水溶液中部分电离的电解质称弱电解质
弱电解质:弱酸:弱酸:CHCH33COOHCOOH、、HH22COCO33、、HClOHClO、、HFHF、、HH22SOSO33、、HH22SS等等弱碱:弱碱:NHNH33·H·H22OO、、Fe(OH)Fe(OH)33、、Cu(OH)Cu(OH)22等等极弱电解质:水(H2O)强酸:强酸:HClHCl、、HH22SOSO44、、HNOHNO33、、HClOHClO44、、HBrHBr等等强碱:强碱:NaOHNaOH、、KOHKOH、、Ca(OH)Ca(OH)22、、Ba(OH)Ba(OH)22等等大多数盐类:AgNO3、KNO3、NH4Cl、Na2CO3等等请写出H2SO4、H2CO3、NHNH33·H·H22OO、、Na2CO3的电离方程式
强电解质弱电解质电离方程式的书写:——完全电离,书写时用“=”号(2)弱