影响化学反应速率的因素回忆:化学反应的碰撞理论:⑴、化学反应的实质是:旧的化学键断裂,新的化学键形成⑵、化学反应发生的先决条件:反应物分子相互接触和碰撞注意:反应物分子之间的碰撞次数很大,但并不是每一次碰撞均可发生化学反应
在化学上,把能够发生化学反应的碰撞叫有效碰撞;不能发生化学反应的碰撞叫无效碰撞;有效碰撞次数越多,反应速率越快
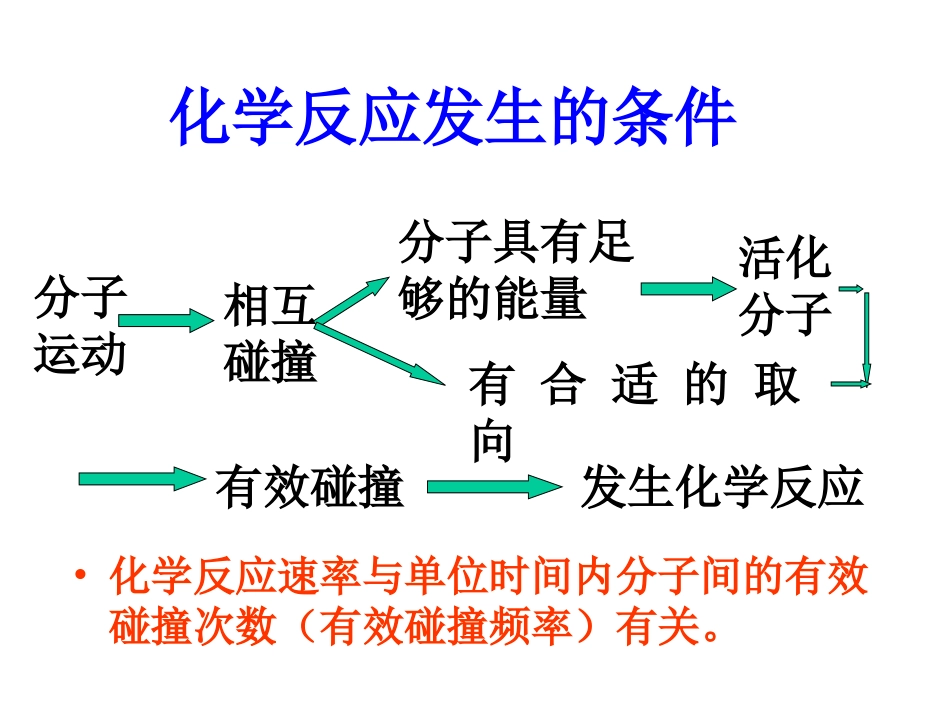
分子运动相互碰撞分子具有足够的能量活化分子有合适的取向有效碰撞发生化学反应化学反应发生的条件•化学反应速率与单位时间内分子间的有效碰撞次数(有效碰撞频率)有关
实验步骤实验现象结论实验二:温度对化学反应速率的影响升高温升高温度反应度反应速率增速率增大大进行加热的先生成沉淀已知:Na2S2O4+H2SO4==Na2SO4+SO2↑+S↓+H2OP21实验2-3三、温度对反应速率的影响由Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2反应同浓度下高温首先出现混浊,说明升温可加速反应升温可加速反应
一般每升高10℃反应速率可增加2~4倍阅读课本实验2-3,总结出温度对化学反应速率的影响
结论:在其它条件不变的情况下,升温反应速率增大,降温反应速率减小为什么
实验2一3•Na2S2O4+H2SO4==Na2SO4+SO2+S↓+H2O•从实验中可以得出结论∶加热的一组首先出现浑浊
•科学探究∶碘化钾加入稀硫酸,振荡加淀粉溶液,加热的试管先出现蓝色
一方面一方面,,升高温度使分子获得更高的能量升高温度使分子获得更高的能量,,活化活化分子百分数提高分子百分数提高;;另一方面另一方面,,升高温度升高温度,,使分子间碰撞频率提高使分子间碰撞频率提高
原理解释原理解释有效碰撞几率提高有效碰撞几率提高,,反应速率增大反应速率增大
在浓度一定时,升高温度,反应物分子的能量增加,使原来一部分原来能量较低的分子变成活化分子,从而增加了反应物分子中