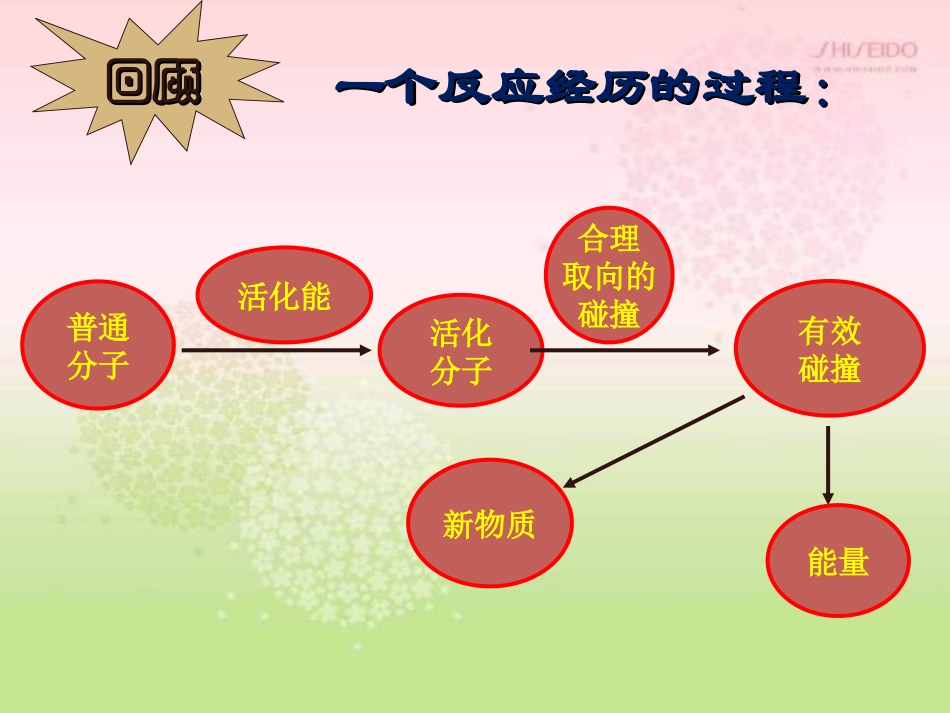
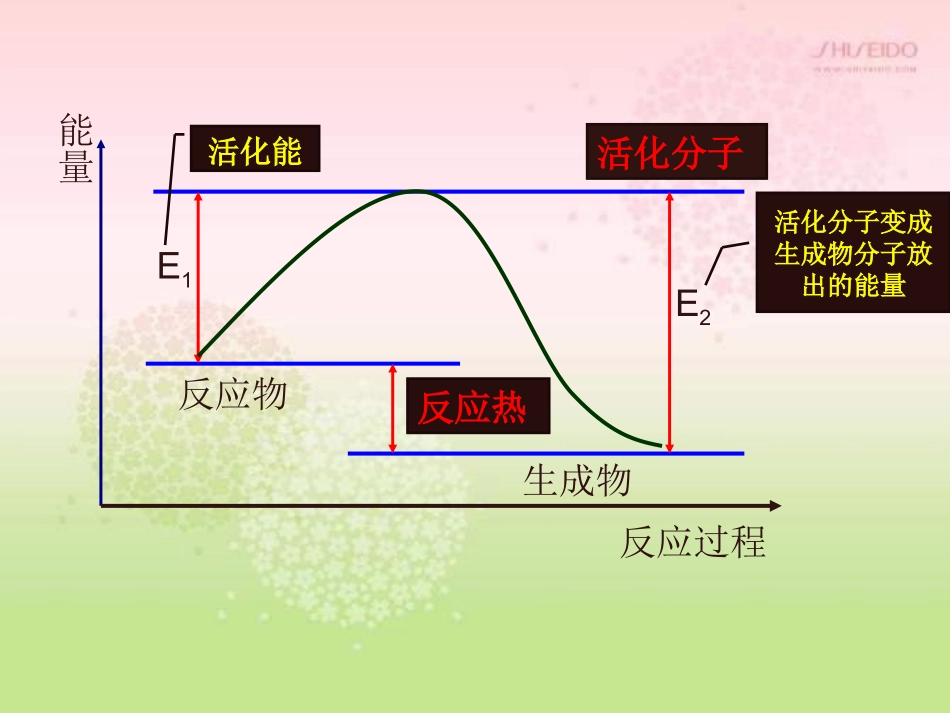
第二节影响化学反应速率的因素普通分子活化能活化分子合理取向的碰撞有效碰撞新物质能量一个反应经历的过程:一个反应经历的过程:回顾回顾能量反应过程E1E2反应物生成物活化分子活化能反应热活化分子变成生成物分子放出的能量(1)碰撞过轻HI分子的几种可能的碰撞模式(2)碰撞取向不好(3)活化分子的有效碰撞反应反应物物本本身的身的性质性质活化活化能能的的大小大小单位单位体积体积内内活活化分化分子子的的多少多少单位单位时间时间内内有有效碰效碰撞撞次次数的数的多少多少化学化学反应反应速率速率快慢快慢决定决定决定决定决定决定决定决定内因内因外因外因第二节影响化学反应速率的因素一、浓度对反应速率的影响实验2-2结论:浓度大的H2C2O4溶液先褪色
2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O结论:其他条件不变,反应物其他条件不变,反应物浓度越大浓度越大化学化学反应反应速率越快速率越快
活化分子百分数=(活化分子数/反应物分子数)×100%浓度增大→单位体积内N活↑T不变,活%不变N活增大→有效碰撞↑→V↑注意事项:1)此规律只适用于气体反应或溶液中气体反应或溶液中的反应,对于纯液体或固体反应物一般情况下其浓度是常数,因此改变它们的量不会改变化学反应速率
一般来说,固体反应物表面积越大,反应速率越大,固体反应物表面积越小,反应速率越小
2)化学反应为可逆反应可逆反应,反应物或生成物浓度的改变,其正反应速率或逆反应速率的变化也符合上述的规律逆反应速率的变化也符合上述的规律
应用2:若将物质的量相等的HI气体分别放在等容积的两个针桶中,一个保持体积不变,另一个压缩为原来的1/2
其它条件不变,则HI的分解反应速率谁快
应用3:如反应:3KSCN+FeCl3=Fe(SCN)3+3KCl若在上述反应体系中加入KCl晶体,会不会影响化学反应速率