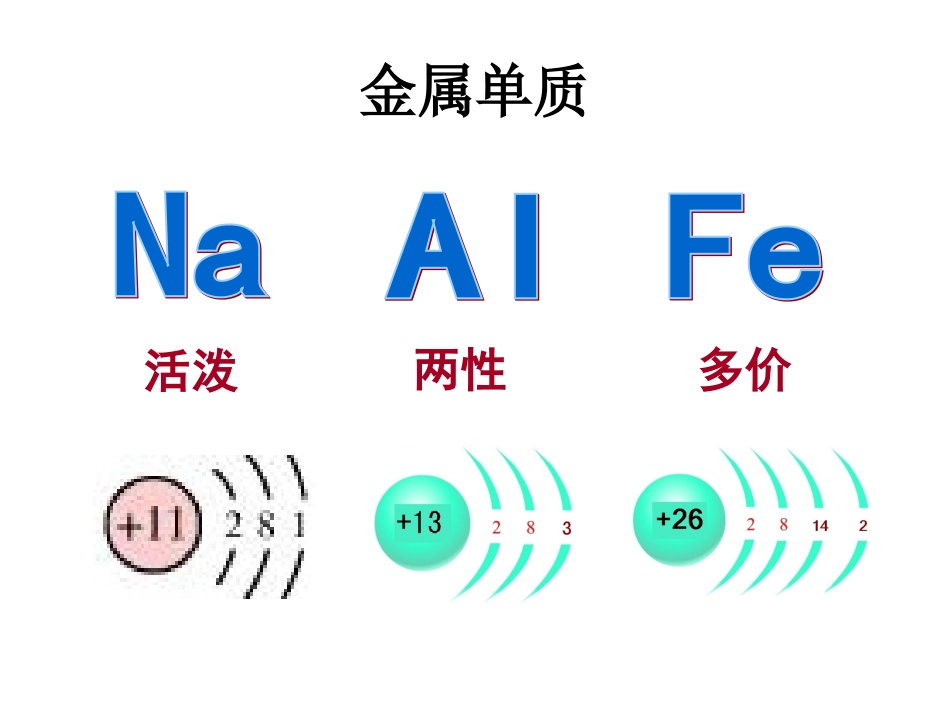
2002年7月7日,在珠江石溪附近,前前后后共漂着七个白色的来历不明的金属桶。突然,从漂在水面上的一个桶中冒起一股白烟,窜起亮黄色火苗,紧接着一声巨响,蘑菇状的水柱冲天而起。这个铁桶接着又连续爆炸了多次,爆炸腾起的白色烟雾有近十米高。图为工作人员小心翼翼的打捞金属桶据悉,另有一金属桶被过往船只发现,并将其打捞上船,打算清洗后使用,但当船员把盖子打开后,桶内立刻冒起浓浓的白烟,一接触桶内物质,双手立即感到剧烈疼痛。于是,他们又将其推到江里,一遇水,这个桶就又爆炸了。第三章复习金属及其化合物金属单质活泼两性多价常见金属活动顺序KCaNaMgAlZnFeSnPbCuHgAgPtAu学习金属的思路:金属氧化物氢氧化物盐研究內容:物理性质化学性质制法用途一、金属的性质1.金属的物理性质:(共性)金属原子的最外层电子排布特点:金属原子最外层电子数较少,易失去最外层电子。2.金属的化学性质金属与非金属、水、酸、盐等反应有金属光泽、易传热、易导电,有延展性、可塑性,常温下除汞(液态)以外都是固体。有还原性(1)与氧气的反应3Fe+2O2==Fe3O4黑色点燃4Al+3O2=2Al2O3Δ4Na+O2=2Na2O白色加热时:淡黄色2Na+O2=Na2O2△钠与氧气:常温下:铝与氧气:铁与氧气:(2)金属与水反应__Na+__H2O=________________KCaNaMgAlZnFeSnPbCuHgAgPtAu与冷水反应与热水反应与水蒸气反应不与水反应2Al+6H2O=2Al(OH)3+3H2↑Δ3Fe+4H2O(g)=Fe3O4+4H2Δ22NaOH+H2↑2(3)与强酸的反应2Na+2HCl=2NaCl+H2↑2Al+6HCl=2AlCl3+3H2↑Fe+2HCl=FeCl2+H2↑KCaNaMgAlZnFeSnPb(H)CuHgAgPtAu金属活动顺序中,H以前的金属和稀酸反应生成盐和氢气H以后的金属不与盐酸、稀硫酸反应(4)与强碱的反应__Al+__NaOH+___H2O=_______________2NaAlO2+3H2↑222(5)与盐溶液的反应Fe+CuSO4=FeSO4+CuNa与CuSO4溶液反应的化学方程式:2Na+CuSO4+2H2O=Na2SO4+Cu(OH)2↓+H2↑注意:活泼金属与盐溶液反应时,首先与水反应,然后与盐反应。金属氧化物氧化物金属氧化物非金属氧化物碱性氧化物两性氧化物其它氧化物:过氧化物酸性氧化物其它氧化物Na2ONa2O2颜色状态氧元素价态生成条件与水反应与CO2反应特性淡黄色固体白色固体-2价常温Na2O+H2O=2NaOH2Na2O2+2H2O=4NaOH+O2↑Na2O+CO2=Na2CO32Na2O2+2CO2=2Na2CO3+O2___氧化物___性氧化物-1价加热加热碱过•Al2O3——两性酸:Al2O3+__HCl=_________________;碱:Al2O3+__NaOH=_________________;62AlCl3+3H2O22NaAlO2+H2OFeOFe3O4Fe2O3颜色Fe化合价能否被氧化到更高价黑色黑色红棕色+2+2和+3+3能能不能Al(OH)3+NaOH=NaAlO2+2H2OFe(OH)2Fe(OH)3Fe的价态+2+3颜色白色红褐色相互转化能否被氧化到更高价能不能Al(OH)3——两性与酸与碱Al(OH)3+3HCl=AlCl3+3H2ONa、Al、Fe的盐•Na2CO3溶解度大、碱性强;•NaHCO3不稳定、与盐酸反应快•Al3+、Fe3+有净水作用物质Na2CO3NaHCO3不同原子团CO32—HCO3—溶解度大小碱性强弱强弱热稳定性稳定不稳定酸HClCO2碱NaOH盐CaCl2相互转化Na2CO3NaHCO3加H:通CO2加H:通CO2去H:加碱、加热去H:加碱、加热2个H+——慢1个H+——快H2ONa2CO3+H2O+CO2=2NaHCO3不反应不反应不反应沉淀★铝盐——KAl(SO4)2·12H2O【思考】如何检验其中的Al3+?明矾向溶液中滴加氢氧化钠,产生白色沉淀,继续滴加氢氧化钠,沉淀先增多后减少,最后消失.★铁盐和亚铁盐的检验1、检验:Fe3+(FeCl3)的检验①用NaOH;②用KSCNFe2+(FeCl2)的检验①用NaOH;②转化为Fe3+再用KSCN检验Fe3+(FeCl3)加KSCN溶液呈红色;加氢氧化钠产生红褐色沉淀.Fe2+(FeCl2)加氢氧化钠产生白色沉淀,而后迅速转化为灰绿色,最后变为红褐色沉淀加KSCN溶液颜色无变化,再加氯水溶液呈红色2FeCl2+Cl2=2FeCl32FeCl3+Fe=3FeCl2除杂焰色反应是表现元素的性质,是物理变化。一根铂丝,将铂丝在一根铂丝,将铂丝在稀盐酸稀盐酸中蘸一下,然中蘸一下,然后在酒精灯火焰上后在酒精灯火焰上灼烧至无色灼烧至无色。用灼烧后的铂丝蘸。用灼烧后的铂丝蘸取少许待测物,火焰中灼烧观察到不同颜色的火焰取少许待测物,火焰中灼烧观察到不同颜色的火焰((KK的焰色要透过钴玻璃观察的焰色要透过钴玻璃观察)。)。...