第四节酸碱盐的应用(第一课时)六、如何稀释浓硫酸六、如何稀释浓硫酸0
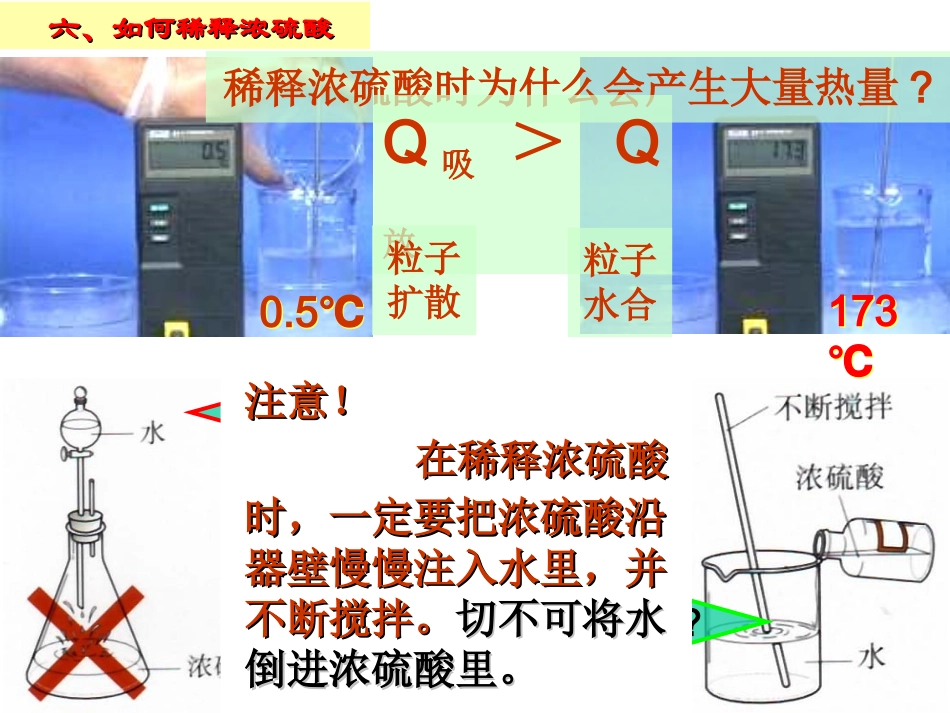
5℃173℃173℃稀释浓硫酸时为什么会产生大量热量
Q吸>Q放粒子扩散粒子水合是将水注入浓硫酸呢
还是将浓硫酸注入水呢
在稀释浓硫酸在稀释浓硫酸时,一定要把浓硫酸沿时,一定要把浓硫酸沿器壁慢慢注入水里,并器壁慢慢注入水里,并不断搅拌
切不可将水切不可将水倒进浓硫酸里
倒进浓硫酸里
六、如何稀释浓硫酸六、如何稀释浓硫酸如果不慎将浓硫酸沾到皮肤或衣服上,应如何处理
如果将稀硫酸沾到皮肤或衣服上,是否也要进行这样的处理
“浓硫酸是无色、无味、粘稠、油状的液体,不挥发,98%的浓硫酸的密度为1
84g/mL,具有强烈的腐蚀性”
请指出其中有哪些性质
有没有化学性质
将两瓶同体积的98%的浓硫酸和10%的稀硫酸区分开来,你能想出哪些不同的方法
甲生:二者的密度小的是稀硫酸,密度大的是浓硫酸,可分别用密度计测它们的密度
乙生:二者的质量不同,质量小的是稀硫酸,质量大的是浓硫酸,可分别用天平称取两种酸的质量
丙生:浓硫酸溶于水会放出大量的热,而稀硫酸则没有那么明显,可分别稀释两种酸,再用手摸外壁,较热的一杯是浓硫酸,另一杯是稀硫酸
主要应用:一判断金属跟酸能否发生置换反应及其反应的快慢
二判断金属跟盐溶液能否发生置换反应
三判断金属跟混合盐溶液反应的次序
金属活动性顺序金属活动性顺序由强逐渐减弱金属活动性顺序由强逐渐减弱KCaNaMgAlZnFeSnPb(H)CuHgAgPtAuKCaNaMgAlZnFeSnPb(H)CuHgAgPtAu一、判断金属跟酸能否发生置换反应及其反应的快慢
反应条件:1
排在氢前面的金属才能置换酸中的氢1
排在氢前面的金属才能置换酸中的氢2
酸指盐酸和稀硫酸,不能用浓流酸,硝酸
酸指盐酸和稀硫酸,不能用浓流酸,硝酸
生成的盐必须可溶