溶液,溶解度专题复习一,配制一定溶质质量分数的溶液1.(2015
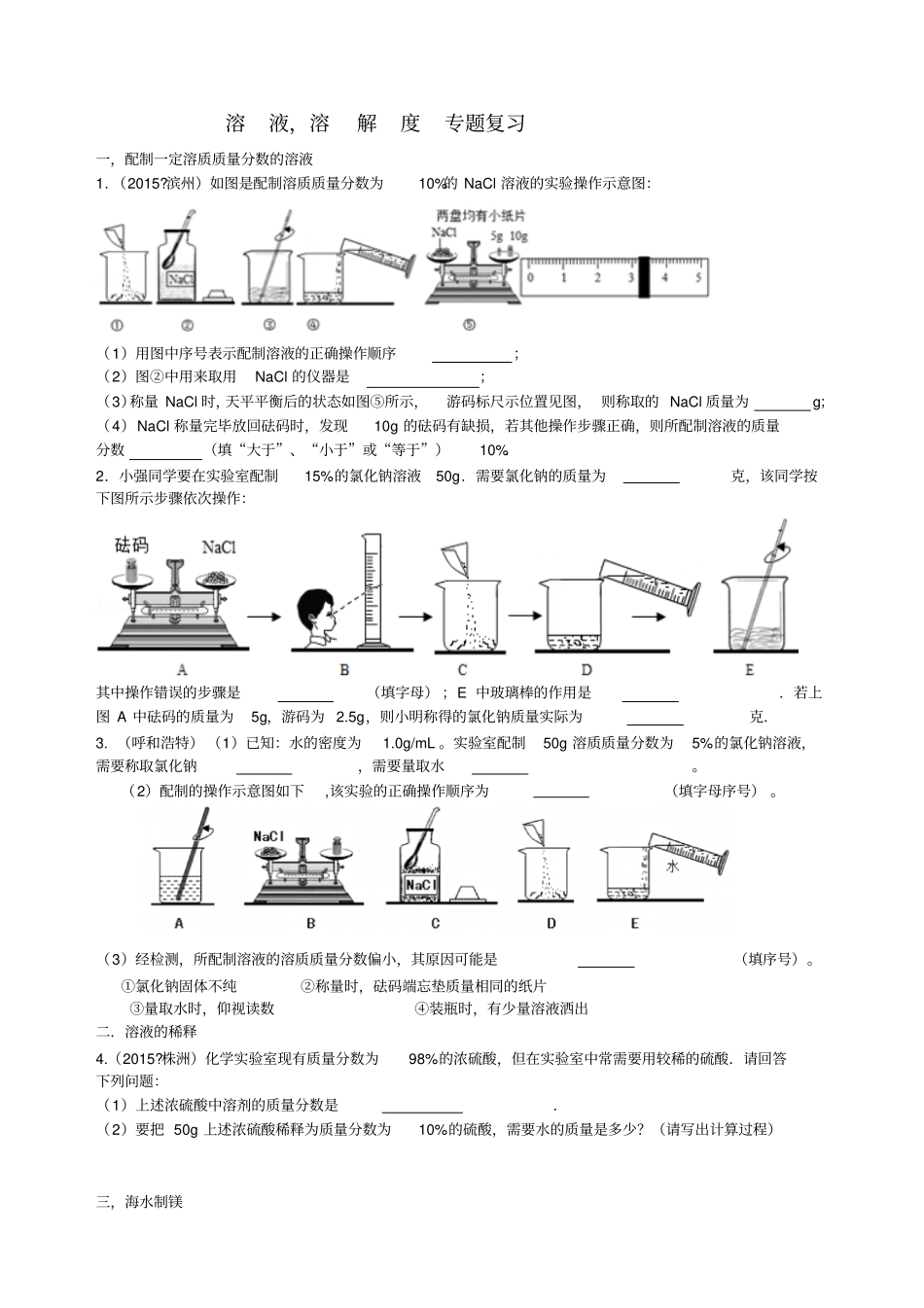
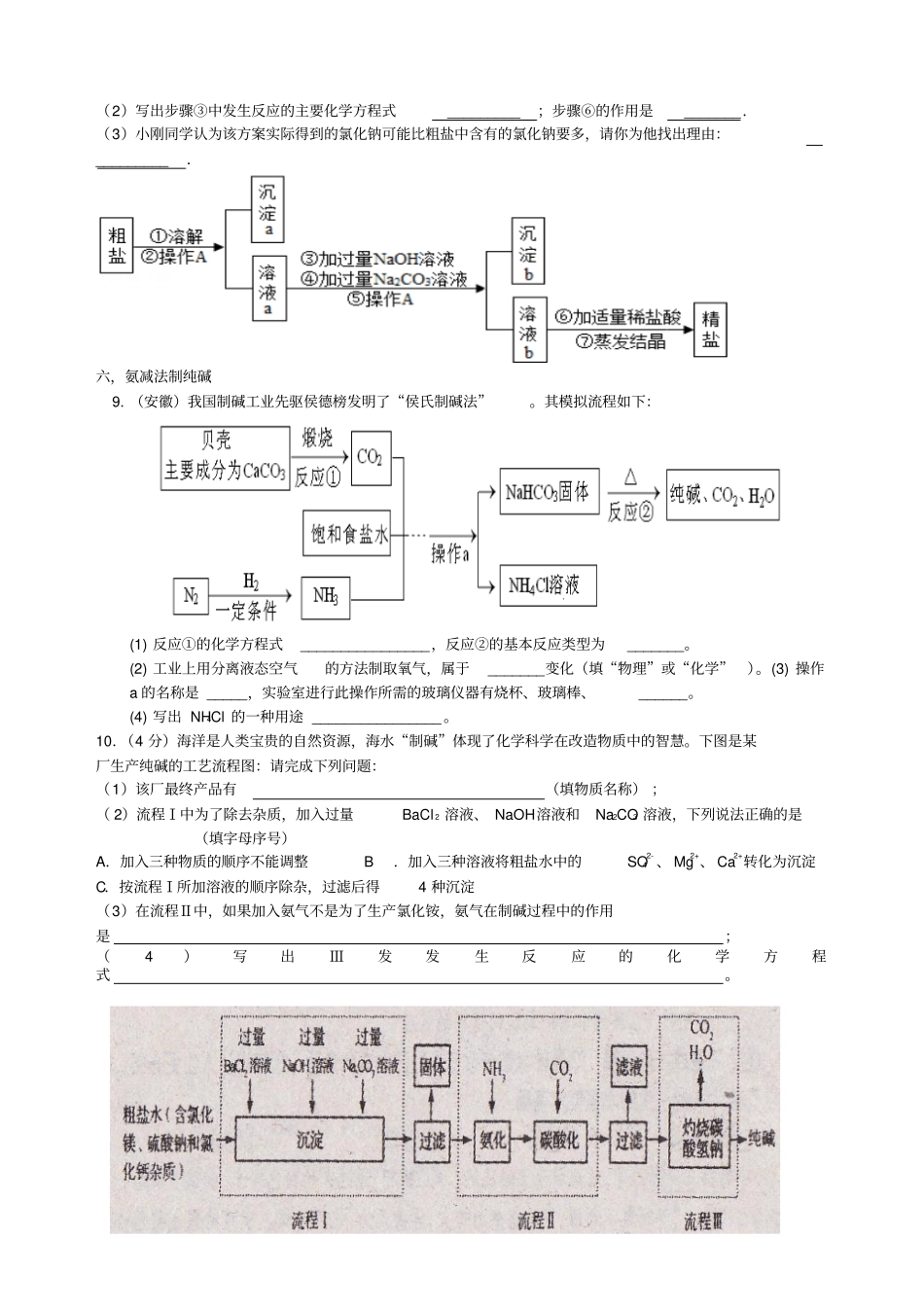
滨州)如图是配制溶质质量分数为10%的NaCl溶液的实验操作示意图:(1)用图中序号表示配制溶液的正确操作顺序;(2)图②中用来取用NaCl的仪器是;(3)称量NaCl时,天平平衡后的状态如图⑤所示,游码标尺示位置见图,则称取的NaCl质量为g;(4)NaCl称量完毕放回砝码时,发现10g的砝码有缺损,若其他操作步骤正确,则所配制溶液的质量分数(填“大于”、“小于”或“等于”)10%.2.小强同学要在实验室配制15%的氯化钠溶液50g.需要氯化钠的质量为克,该同学按下图所示步骤依次操作:其中操作错误的步骤是(填字母);E中玻璃棒的作用是.若上图A中砝码的质量为5g,游码为2
5g,则小明称得的氯化钠质量实际为克.3
(呼和浩特)(1)已知:水的密度为1
实验室配制50g溶质质量分数为5%的氯化钠溶液,需要称取氯化钠,需要量取水
(2)配制的操作示意图如下,该实验的正确操作顺序为(填字母序号)
(3)经检测,所配制溶液的溶质质量分数偏小,其原因可能是(填序号)
①氯化钠固体不纯②称量时,砝码端忘垫质量相同的纸片③量取水时,仰视读数④装瓶时,有少量溶液洒出二.溶液的稀释4
株洲)化学实验室现有质量分数为98%的浓硫酸,但在实验室中常需要用较稀的硫酸.请回答下列问题:(1)上述浓硫酸中溶剂的质量分数是.(2)要把50g上述浓硫酸稀释为质量分数为10%的硫酸,需要水的质量是多少
(请写出计算过程)三,海水制镁5
株洲)镁是一种用途很广的金属,目前世界上60%的镁是从海水(主要含NaCl和MgCl2等)中提取的.主要步骤如下:(1)上述步骤中试剂①应过量,理由是.(2)请写出Mg(OH)2沉淀与试剂②发生中和反应的化学方程式.(3)无水MgCl2在熔融状态下通电得到金属镁和物质A,氢