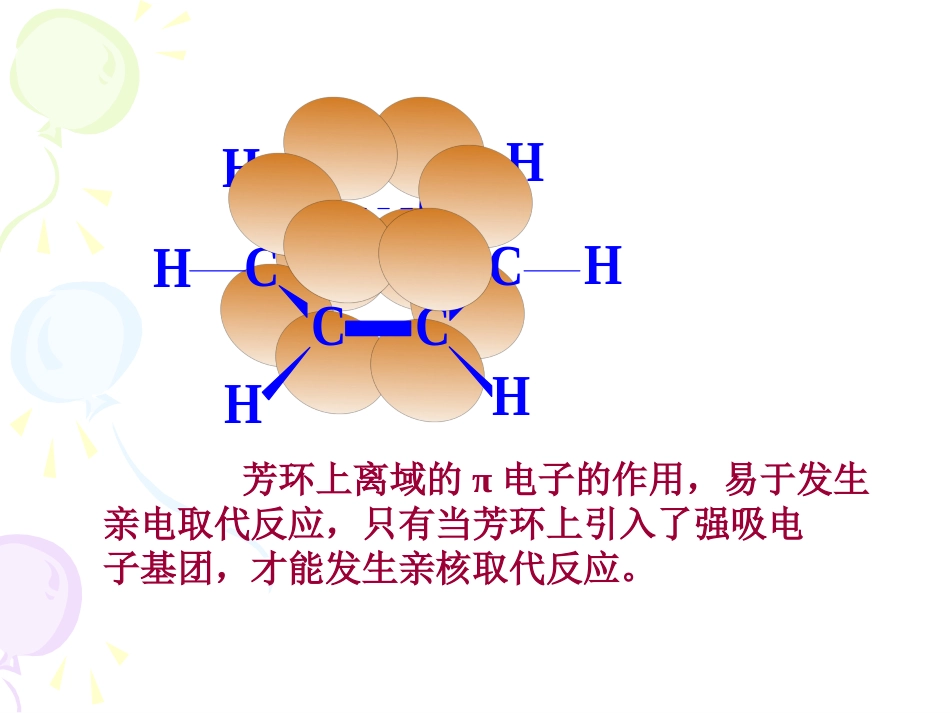
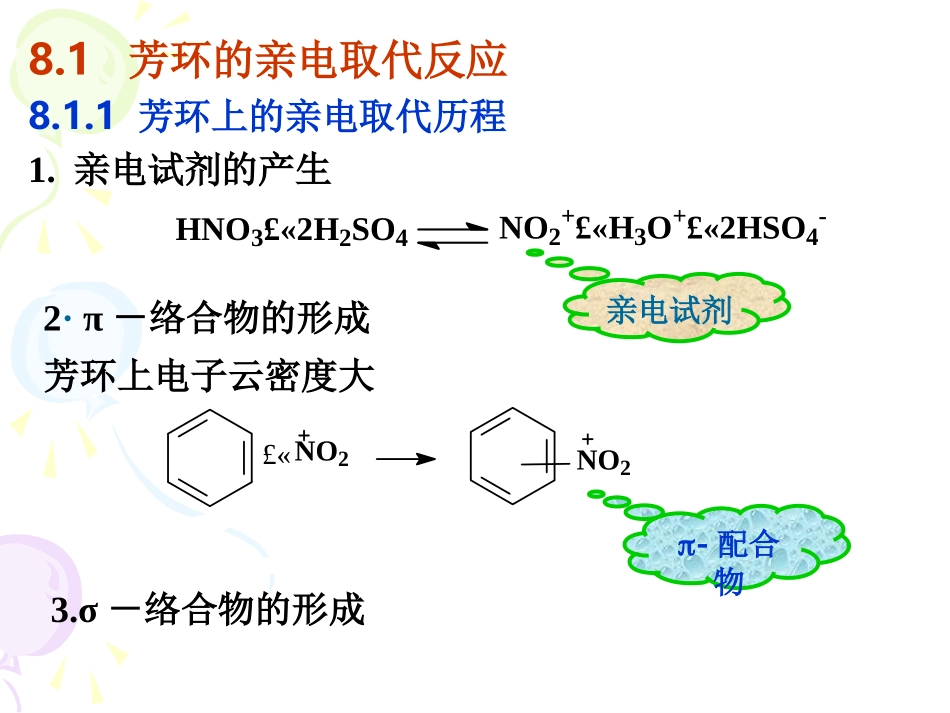
第八章芳环上的亲电第八章芳环上的亲电和亲核取代反应和亲核取代反应CCCCCCHHHHHH芳环上离域的π电子的作用,易于发生亲电取代反应,只有当芳环上引入了强吸电子基团,才能发生亲核取代反应
1芳环的亲电取代反应8
1芳环上的亲电取代历程1
亲电试剂的产生HNO3£«2H2SO4NO2+£«H3O+£«2HSO4-亲电试剂2·π-络合物的形成芳环上电子云密度大£«NO2NO2-配合物3
σ-络合物的形成NO2+HNO2¦Ò£ÂçºÏÎïÂýsp3杂化4
消去H+,恢复芳环的Kekulè结构HNO2-H+NO2¿ìσσ-络合物的证据-络合物的证据CH3£«CH3CH2F£«BF3CH3CH2CH3HBF4-通过红外和核磁等可鉴定其结构芳香稳定性¡÷CH3EtCH3CH3mp-15C黄色CH3CH3CH3EtFBF3,-80¡æCH3HEtCH3CH3BF4-加成--消除历程σ-络合物生成是决定反应速率的步骤这种机理称:Ar-SE8
2苯环上亲电取代反应的定位规律从反应速度和取代基进入的位置进行考虑1
第一类定位基(邻、对位定位基)Ö»î»ùNH2NHRNR2OHORNHCROPhRFClBrIÖ¶ۻù-I+C2
第二类定位基(间位定位基)均为致钝基均为致钝基NO2NR3COOHCOORSO3HCNCHOCROCCl38
3定位规律在有机合成中的应用8
4典型的芳香亲电取代反应1
硝化反应HNO3-H2SO4为常见的硝化试剂HNO3£«2H2SO4NO2+£«H3O+£«2HSO4-真正的硝化试剂混酸体系有强氧化性OH20%HNO3OHNO2£«OHNO2如用混酸将得氧化产物同时还有部分氧化产物同时还有部分氧化产物NH2ŨHNO3ŨH2SO4NH3HSO4-NO2HNO3/CCl4低温时的硝化速度较快OCH3£«HNO3CH3COOHCH3ONO2