1、单质碳的性质和主要用途
本单元重点、难点:复习策略:比较学习法的运用3、二氧化碳和一氧化碳的化学性质及用途
2、实验室中制取二氧化碳的反应原理及装置
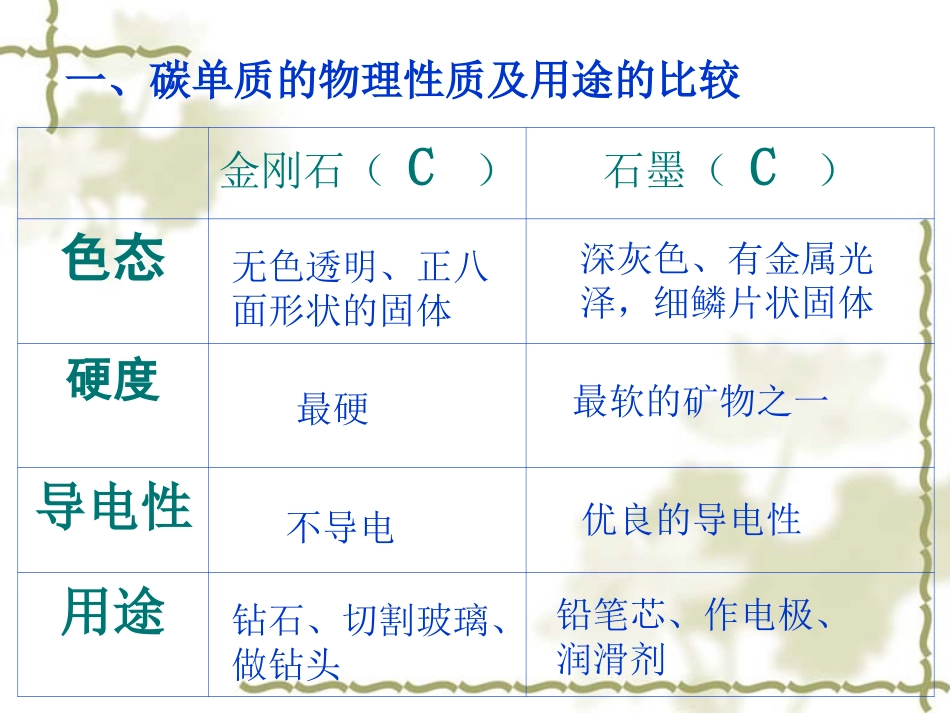
金刚石(C)石墨(C)色态硬度导电性用途无色透明、正八面形状的固体最硬深灰色、有金属光泽,细鳞片状固体最软的矿物之一不导电优良的导电性钻石、切割玻璃、做钻头铅笔芯、作电极、润滑剂一、碳单质的物理性质及用途的比较金刚石、石墨都是由碳元素组成的单质,为什么它们的物理性质差异那么大呢
思考:碳原子的排列方式不同决定决定反映反映物质的结构物质的性质物质的用途1、5克的金刚石和5克的石墨组成的物质是()A、纯净物B、混合物2、石墨在一定条件下可转化为金刚石,该变化是()A、物理变化B、化学变化BB巩固练习3、继发现C60后C70也已经制得,下列有关C70的说法正确的是()A
它是一种化合物B
它是一种单质,并且它是有C70分子构成的
它是一种混合物D
它的相对分子质量是840B、D巩固练习化学性质用途单质碳常温高温时制墨水作燃料冶炼金属可燃性还原性稳定2C+O22CO(O2不充足)C+O2CO2(O2充足)点燃点燃C+2CuO2Cu+CO2高温二、单质碳化学性质及用途的比较碳和某些氧化物的反应:黑色粉末变成红色粉末澄清石灰水变浑浊
现象:C+2CuO2Cu+CO2高温2Fe2O3+3C4Fe+3CO2高温三、二氧化碳和一氧化碳CO2CO物理性质颜色状态密度溶解性收集方法无色无味气体,固体为干冰无色无味气体比空气大与空气相差不大能溶于水难溶于水只能用向上排空气法收集只能用排水法收集物质一氧化碳二氧化碳化学性质可燃性还原性与水反应与石灰水反应毒性点燃2CO+O2===2CO2既不能燃烧也不能支持燃烧△CO+CuO===Cu+CO2无无H2O+CO2===H2CO3无Ca(OH)2+CO2===H2O+CaCO3↓剧毒无物质一氧化碳二