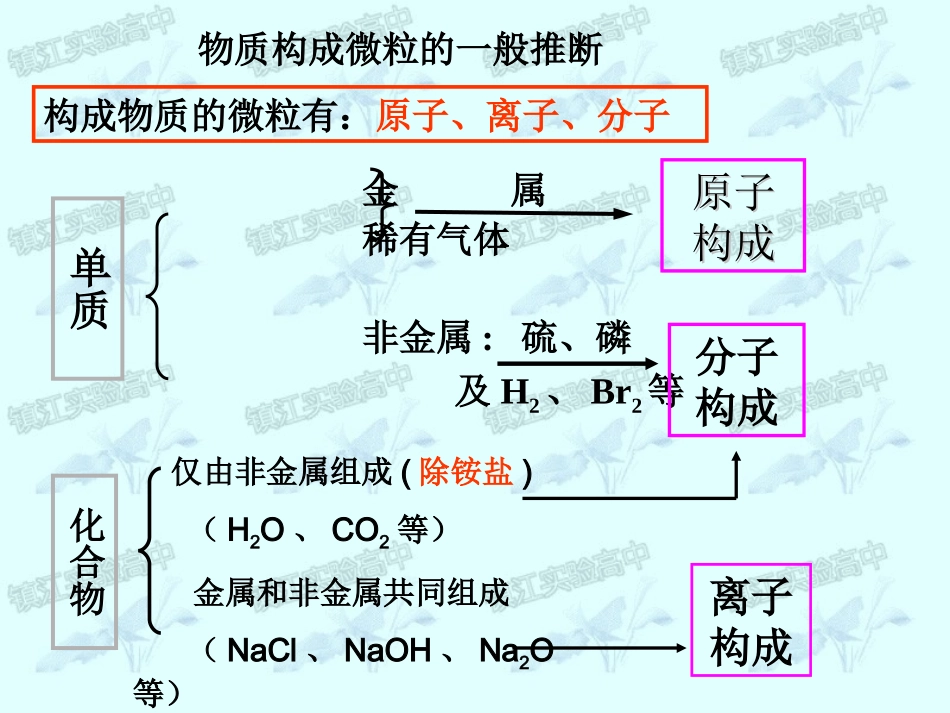
第三单元人类对原子结构的认识第一课时:一、原子结构模型的演变二、原子核外电子的排布三、原子的构成专题1化学家眼中的物质世界物质构成微粒的一般推断金属稀有气体非金属:硫、磷及H2、Br2等原子原子构成构成分子构成单质化合物仅由非金属组成(除铵盐)(H2O、CO2等)金属和非金属共同组成(NaCl、NaOH、Na2O等)离子构成构成物质的微粒有:原子、离子、分子时间科学家名称模型特点公元前5世纪古希腊哲学家原子万物是由大量的不可分割的微粒构成的1803道尔顿实心球原子是坚实不可再分的微小实心球1904汤姆生葡萄干面包式正电荷内镶嵌着电子1911卢瑟福带核的模型原子核位于中心,电子在核周围高速运动1913玻尔壳层模型电子在核外空间的一系列轨道上绕核做高速运动1926海森伯等量子力学模型用量子力学方法描述核外电子的运动一、原子结构模型的演变微观电子的特征1
电子的质量很小,只有9
11×10-31千克;2
核外电子的运动范围很小(相对于宏观物体而言);3
电子的运动速度很大;二、原子核外电子的排布1、多电子原子里,电子在核外分层排布的原子与原子核大型体育场与蚂蚁电子层的表示方法:12345……KLMNO……离核由近到远,能量由低到高小结:电子层不但表示离核的远近,而且还表示电子能量的高低
(2)最外层电子数不超过8个(K层为最外层时,最多不超过2个)
(3)次外层电子数目不超过18个,倒数第三层不超过32个
2、原子核外电子的排布规律(1)每层最多容纳2n2个电子(4)能量最低原理:第第11层最多排层最多排22个电子个电子,,填满K层再填L层,第第22层最多排层最多排88个填满个填满LL层后再填层后再填MM层层电子总是尽先排布在能量最低的电子层里+15第1层第2层第3层K层L层M层原子核原子核带正电质子数2853、原子结构示意图1-18号元素的核外电子排布原子结构示意图交流讨论:1