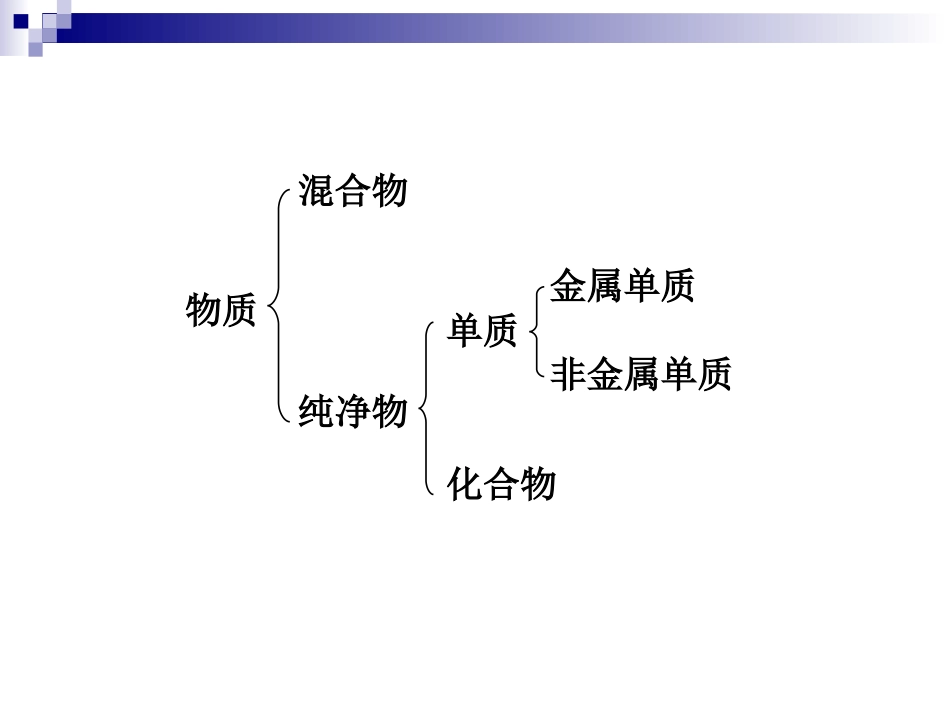
酸碱盐在水溶液中的电离物质混合物纯净物单质化合物金属单质非金属单质导电性金属单质:导电非金属单质:大部分不导电氯化钠、硝酸钾、氢氧化钠溶液蒸馏水、蔗糖的水溶液不导电导电不导电氯化钠、硝酸钾、氢氧化钠、蔗糖固体物质混合物纯净物单质化合物金属单质非金属单质(在一定条件下是否导电)电解质非电解质一、电解质和非电解质电解质:在水溶液或熔融状态下能导电的化合物非电解质:在水溶液和熔融状态下都不能导电的化合物2、电解质和非电解质研究的是化合物,单质和混合物既不是电解质也不是非电解质1、电解质导电外界条件:①在水溶液中②在熔融状态下注意:例1:Cu能导电吗
Cl2的水溶液能导电,Cu和Cl2是电解质吗
Cu导电:Cu中有自由移动的电子Cl2水溶液导电:Cl2+H2O=HClO+HCl发生化学反应才导电的Cu和Cl2既不是电解质,也不是非电解质3、电解质应是在一定条件下本身电离而导电的化合物例3:SO3、SO2、CO2溶于水能导电,那么能说SO3、SO2、CO2是电解质吗
SO3+H2O=H2SO4SO2+H2O=H2SO3CO2+H2O=H2CO3H2SO4、H2SO3、H2CO3是电解质,SO3、SO2、CO2是非电解质例2:NaCl溶液能导电,能否说NaCl溶液是电解质吗
不能,NaCl溶液是NaCl的水溶液,是混合物,不属于化合物,不是电解质二、电解质的类型酸、碱、盐、少数金属氧化物(Na2O、CaO)、水练习:1、下列物质属于电解质的一组是()A.CO2、SO2、HClB.H2SO4、K2O、BaSO4C.H3PO4、H2O、CuD.NH3、CH4、NaClB例4:BaSO4、AgCl、CaCO3这些盐难溶于水,它们是否是电解质
虽然在水溶液中导电性很小,但在熔化状态下这些物质都能导电特别注意:特别注意:Na2ONa2O+H2O=2NaOH(不能判断)Na2O2Na++O2-熔融