第十单元酸和碱物质有分类,溶液有酸碱
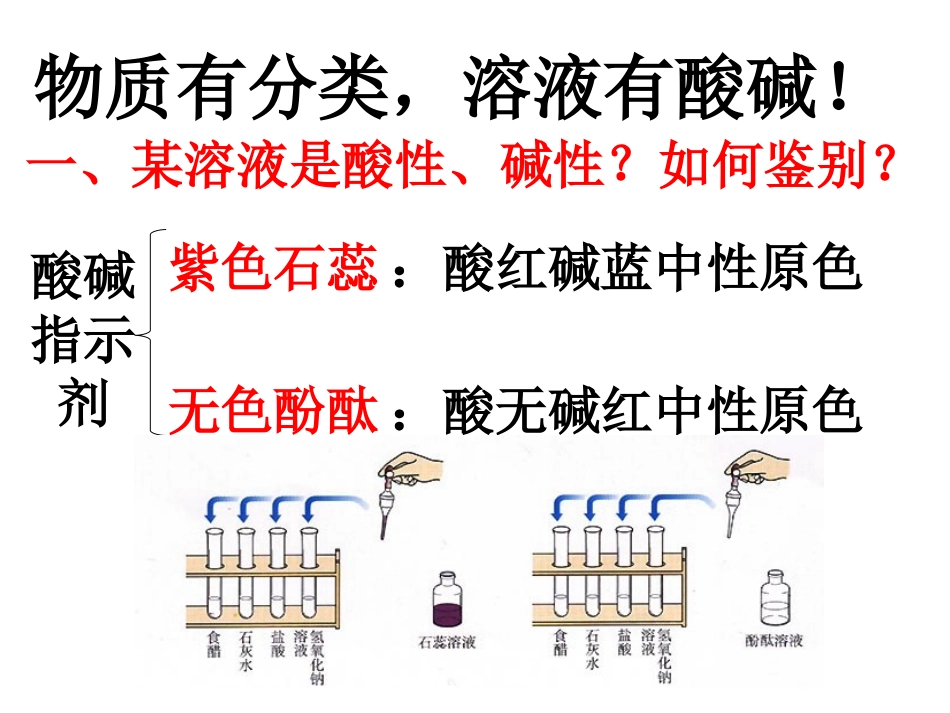
一、某溶液是酸性、碱性
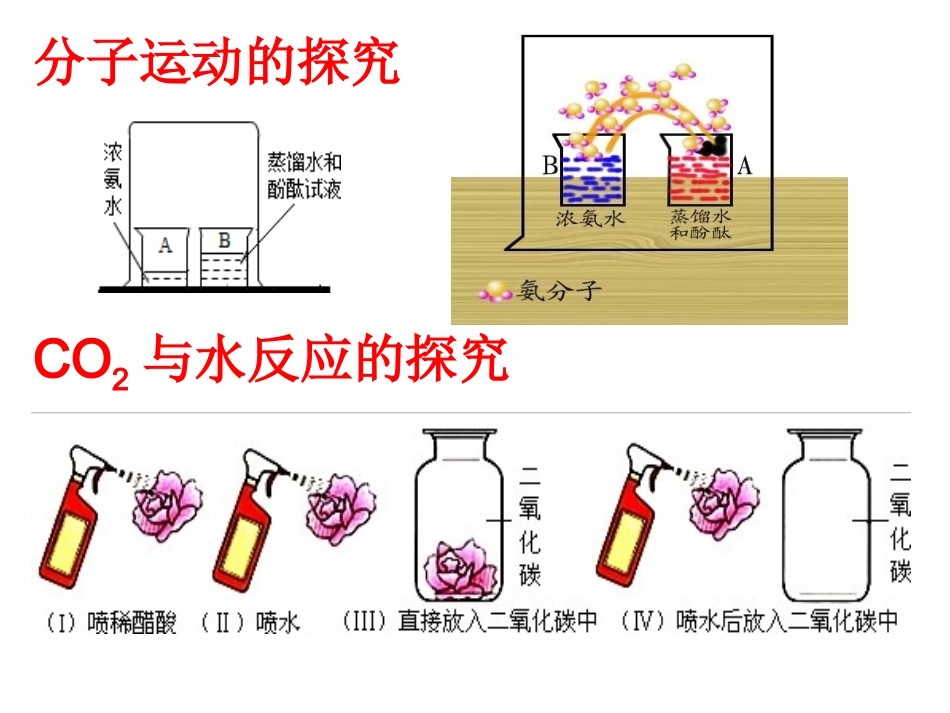
酸碱指示剂紫色石蕊无色酚酞:酸红碱蓝中性原色:酸无碱红中性原色分子运动的探究CO2与水反应的探究二、常见的酸1、盐酸:氯化氢的水溶液,酸碱盐中唯一混合物(胃酸HCl)2、硫酸:S+O2===SO2点燃SO2+O2===SO3PtSO3+H2O==H2SO4(1)酸除渍(锈)、碱除油
(腐蚀性)(2)浓硫酸有吸水性(可做干燥剂)浓硫酸还有脱水性(化学变化)浓硫酸稀释放出大量的热(水沸腾)P53(记忆)三、酸的化学性质1、指示剂2、金属+酸=盐+H2O3、金属氧化物+酸=盐+H2O4、碱+酸=盐+H2O5、盐+酸=新盐+新酸:酸使石蕊变红,酚酞原色Zn+H2SO4=ZnSO4+H2↑Fe2O3+6HCl=2FeCl3+H2O2NaOH+H2SO4=Na2SO4+2H2OAgNO3+HCl=AgCl↓+HNO3BaCO3+H2SO4=BaSO4↓+H2O+CO2↑四、常见的碱1、氢氧化钠:苛性钠、火碱、烧碱暴露在空气中易吸水(做干燥剂)NaOH先潮解(吸水)后反应(与CO2)2、氢氧化钙:熟石灰、消石灰、石灰水石灰乳、石灰浆CaCO3===CaO+CO2↑CaO+H2O=Ca(OH)2Ca(OH)2微溶于水,溶液能吸收空气中CO2酸除渍、碱除油
NaOH:肥皂、造纸、印染、除油污Ca(OH)2:农药、改良土壤、刷墙高温五、碱的化学性质1、指示剂:碱使石蕊变蓝,酚酞变红2、非金属氧化物+碱=盐+H2OCO2+Ca(OH)2=CaCO3↓+H2OCO2+2NaOH=Na2CO3+H2OSO3+2NaOH=Na2SO4+H2O4、碱+盐=新碱+新盐2NaOH+CuSO4=Cu(OH)2↓+Na2SO43KOH+FeCl3=Fe(OH)3↓+3KCl3、碱+酸=盐+H2O2NaOH+H2SO4=Na2SO4+2H2O