物质的量和溶解度本讲内容按知识的内在联系及应用特点可分为二部分
一是以物质的量为中心的各量间的关系及其计算,二是掌握溶解度的计算和溶解度与溶液浓度的相互求算
而学好本章的关键是以正确理解有关的基本概念为前提,建立起以物质的量为核心的化学计算体系,并注重分析溶液的形成过程,准确地判断溶质的物质的量,溶液体积和溶液中其他量的关系,构建起相应的比例关系,从而掌握物质的量和溶解度的计算,达到提高解题和应用知识的能力
[基础知识]一
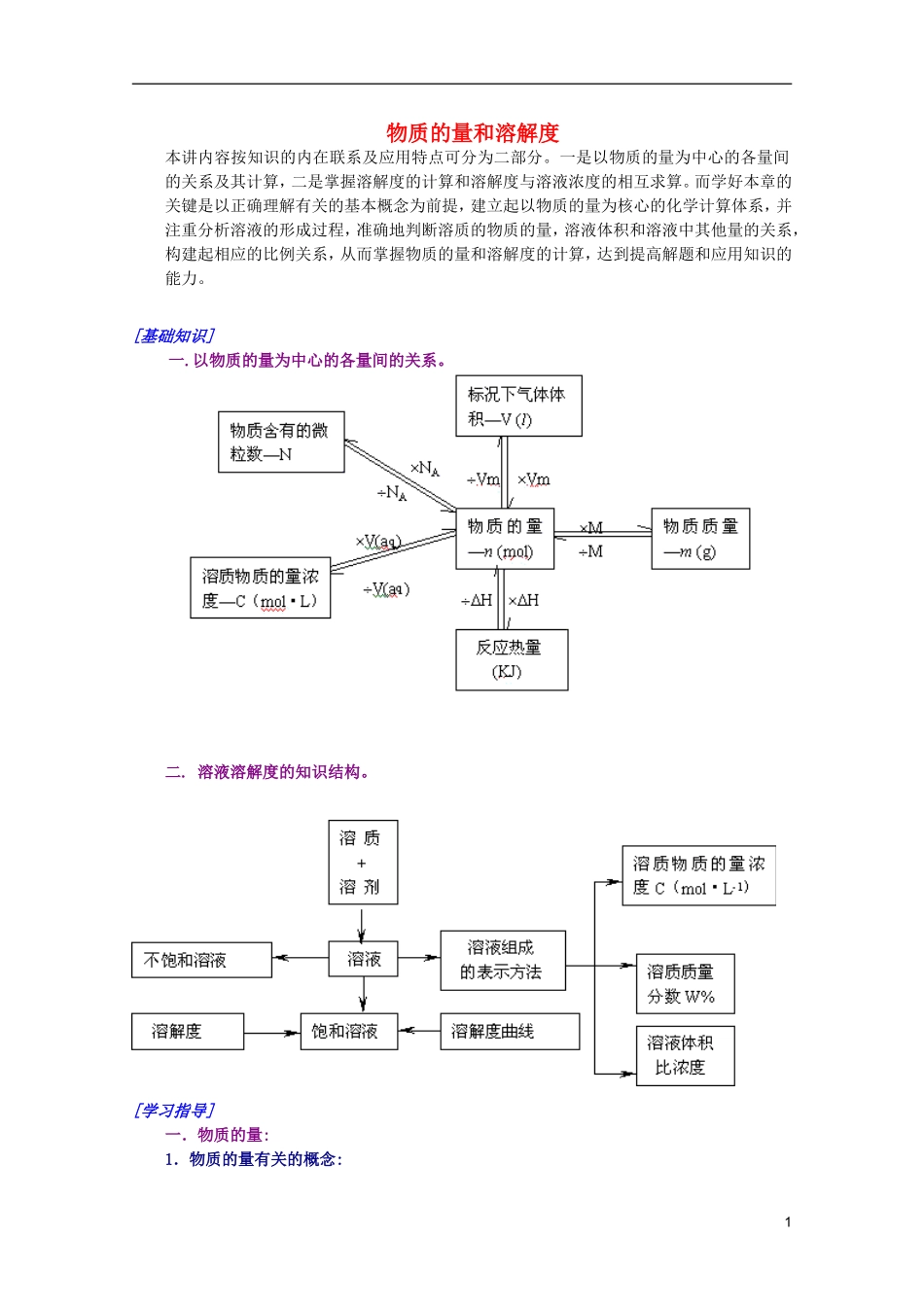
以物质的量为中心的各量间的关系
溶液溶解度的知识结构
[学习指导]一.物质的量:1.物质的量有关的概念:1物质的量在化学计算中处于核心的地位,与它相关的概念有五个
(1)物质的量(n)以0
012kg所含的原子数目即阿伏加德罗常数NA(近似值6
02个mol-1)为计数标准,用来表示物质(或一定量微粒集体中)所含粒子数目(N)多少的物理量
摩尔(mol)是它的单位
每摩尔物质含阿伏加德罗常数个微粒
使用摩尔为单位,必须指明粒子的种类,它们可以是分子、原子、离子、电子、质子和中子等微粒或这些粒子的特定组合
物质的量与粒子数关系:(2)摩尔质量(M)单位物质的量的物质所具有的质量,单位g·mol-1或kg·mol-1
1mol任何粒子或物质的质量以克为单位时在数值上都与该粒子相对原子质量或相对分子质量相等
物质的量与物质质量关系:(3)气体摩尔体积(Vm)在标准状况下,单位物质的量的气体所占有的体积,单位L·mol-1或m3·mol-1
大量实验证明,标况下,1mol任何气体所占的体积都约为22
4L,因此,我们可以认为22
4L·mol-1是特定条件下的气体摩尔体积
气体物质的量与气体体积关系:(4)溶质物质的量浓度(CB)单位体积溶液里所含溶质B的物质的量来表示溶液组成的物理量,单位mol·L-1或mol·m-3
溶质的物质的量和溶液中溶质的物质的量