3343【考纲要求】电化学教学设计(3)N牺牲阳极保护法
【自主纠错】1
理解原电池原理,初步了解化学电源
了解化学腐蚀与电化学腐蚀及一般防腐蚀的方法
理解电解原理,了解氯碱工业,铜的精炼,镀铜反应原理
原电池,电解原理的应用
【学习目标】1
训练解题技巧和答题的规范性
熟练利用原电池和电解池的知识,解决实际问题
【学习难点】电极反应式书写【标准答案】1-7DABCDDD8.(1)b、d(2)Cu2S4氢气(3)aNO-+e-+2H+=NO2↑+H2O(4)做电解质溶液(或导电)9
I、(1)2O2+4H2O+8e-=8OH-CH4+10OH--8e-=CO2-+7H2O(2)H22Cl-+2H2OError:Referencesourcenotfound2OH-+H2↑+Cl2↑(3)4II、(1)负电解2Cl--2e-===Cl2↑Ag++e-===Ag(2)0
025mol·L-1(3)1310
(1)NaOH(2)氯气与水反应:Cl2+H2OHCl+HClO,增大HCl的浓度可使平衡逆向移动,减少氯气在水中的溶解,有利于氯气的溢出
(3)①Mg(OH)2②SO2-、Ca2+11
(1)①2Al+2OH-+6H2OError:Referencesourcenotfound2[Al(OH)4]-+3H2↑b②2Al+3H2O-6e-Error:ReferencesourcenotfoundAl2O3+6H+因为Al3+和HCO—发生了互促水解,Al3++3HCO3-Error:ReferencesourcenotfoundAl(OH)3↓+3CO2↑(合理即得分)(2)补充溶液中消耗的Cu2+,保持溶液中Cu2+的浓度恒定【重点讲解】一、1题、11题(3)
知识点:电化学解题思路,先看有无直流电源
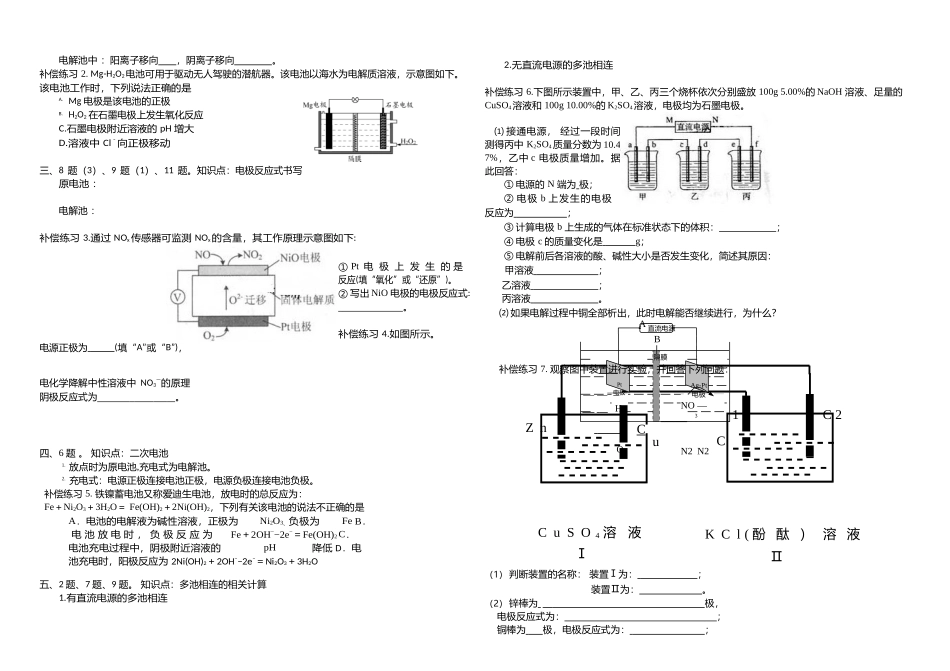
原电池:电解池:补偿练习1
右图所示装置中发生反应的离子方程