高中化学优秀课件:第三章第二节《水的电离和溶液的酸碱性》(人教版选修4)第二节水的电离和溶液的酸碱性一、水的电离1
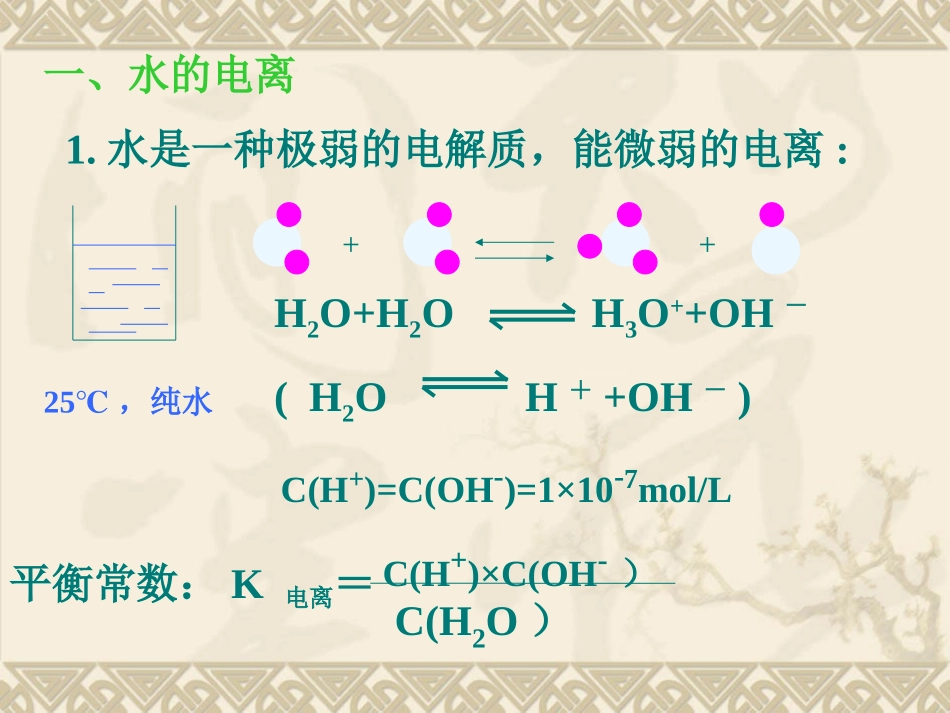
水是一种极弱的电解质,能微弱的电离:25℃,纯水++H2O+H2OH3O++OH-(H2OH++OH-)C(H+)=C(OH-)=1×10-7mol/L平衡常数:K电离=C(H+)×C(OH-)C(H2O)1升纯水的物质的量是55·6mol,经实验测得250C时,发生电离的水只有1×10-7mol,二者相比,水的电离部分太小,可以忽略不计
因此电离前后水的物质的量几乎不变,可以视为常数,常数乘以常数必然为一个新的常数,用Kw表示,即为水的离子积常数,简称水的离子积
在一定温度时:C(H+)×C(OH-)=Kw,叫水的离子积25℃时,Kw=1×10-142
水的离子积水的浓度为常数,所以KW=C(H+)×C(OH-)提问:根据前面所学知识,水的离子积会受什么外界条件影响
KW叫做水的离子积常数,简称水的离子积
特别提示:此时的[H+]和[OH-]是溶液中的总量
KW只是温度的函数(与浓度无关)温度升高,KW值增大如:KW25℃=10-14KW100℃=10-12分析下表中的数据有何规律,并解释之讨论:温度0℃20℃25℃50℃100℃Kw1
14×10-156
81×10-151×10-145
47×10-141×10-12结论:温度越高,Kw越大,水的电离是一个吸热过程水是一种极弱的电解质(通常的电流表无法检验其中离子)注意:1
任何水溶液中H+和OH-总是同时存在的,只是相对含量不同
常温下,任何稀的水溶液中C(H+)×C(OH-)=1×10-143
不论是在中性溶液还是在酸碱性溶液,水电离出的C(H+)=C(OH-)4
根据Kw=C(H+)×C(OH-)在特定温度下为定值,C(H+)和C(OH-)可以互求
1mol/L的盐酸