溶解度【主要内容】饱和溶液和不饱和溶液以及溶解度的理解和应用【知识要点】一、饱和溶液和不饱和溶液1、定义:在一定温度下,向一定量溶剂里加入某种溶质,当溶质不能继续溶解时,所得的溶液叫做饱和溶液,还能继续溶解的溶液叫做不饱和溶液
说明:(1)饱和溶液二要素:“一定温度下”“一定量的溶剂”
(2)某物质的饱和溶液中还可以继续溶解其它物质
(3)如何判断某溶液是否饱和
向该溶液中加入少量的溶质,看能否继续溶解
2、不饱和溶液与饱和溶液间的相互转化:特殊:Ca(OH)2溶解于水时,温度越高,溶解越少;温度越低,溶解越多
3、结晶:(1)定义:溶质从饱和溶液中以晶体的形式析出的过程(2)有晶体析出后的溶液叫母液,它一定是饱和溶液
(3)结晶的方法:a
冷却热饱和溶液人们利用以上的原理从海水中提取食盐并得到含有大量化工原料的母液(叫苦卤)其大致过程如下:问题:你认为它是通过什么方法获得食盐晶体的
——蒸发溶剂[知识拓展]二、溶解度(一)固体溶解度1.概念:在一定温度下,某固态物质在100g溶剂(通常溶剂为水)里达到饱和状态时所溶解的质量
溶解度的概念包括四个要素:①指明一定温度;②溶剂为100g;③必须达到饱和状态;④单位为g
影响固体溶解度的外界因素:温度2.“易溶”、“可溶”、“微溶”、“难溶”等表示的意思:主要是看该物质在200C时这种物质的溶解度:溶解度/g>101~100
01~1<0
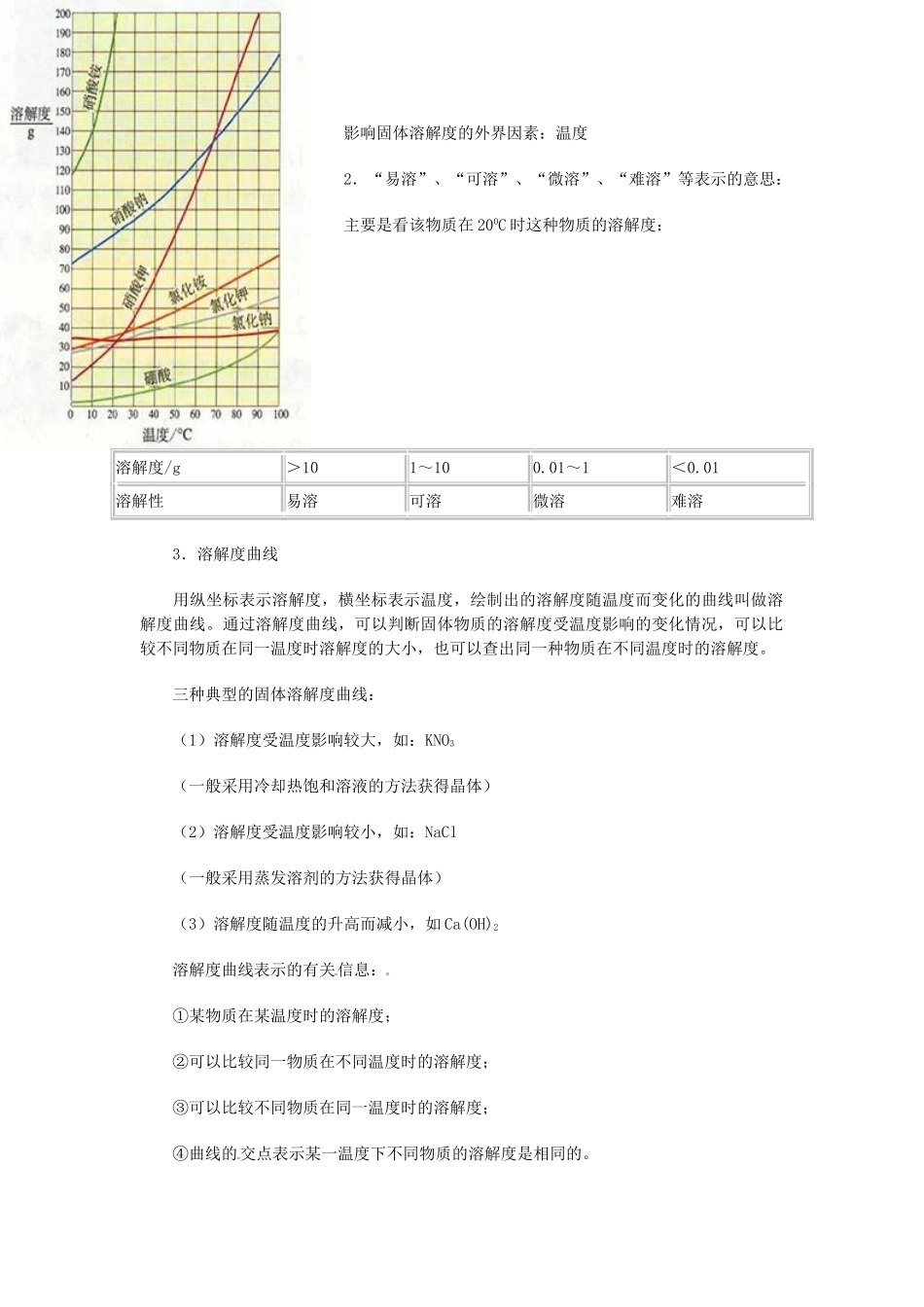
01溶解性易溶可溶微溶难溶3.溶解度曲线用纵坐标表示溶解度,横坐标表示温度,绘制出的溶解度随温度而变化的曲线叫做溶解度曲线
通过溶解度曲线,可以判断固体物质的溶解度受温度影响的变化情况,可以比较不同物质在同一温度时溶解度的大小,也可以查出同一种物质在不同温度时的溶解度
三种典型的固体溶解度曲线:(1)溶解度受温度影响较大,如:KNO3(一般采用冷却热饱和溶液的方法获得晶体)(2)溶