了解电解质、非电解质、强电解质、弱电解质的概念,并能进行判断
2.了解电解质的电离,能够书写电离方程式
3.了解离子反应的概念,掌握离子反应发生的条件
4.掌握离子反应方程式的书写方法
5.能够判断离子方程式的正误和离子共存问题
第二节电解质和离子反应1.电解质与非电解质(1)电解质:在下能够导电的叫做电解质
(2)非电解质:在下都不导电的化合物叫做非电解质
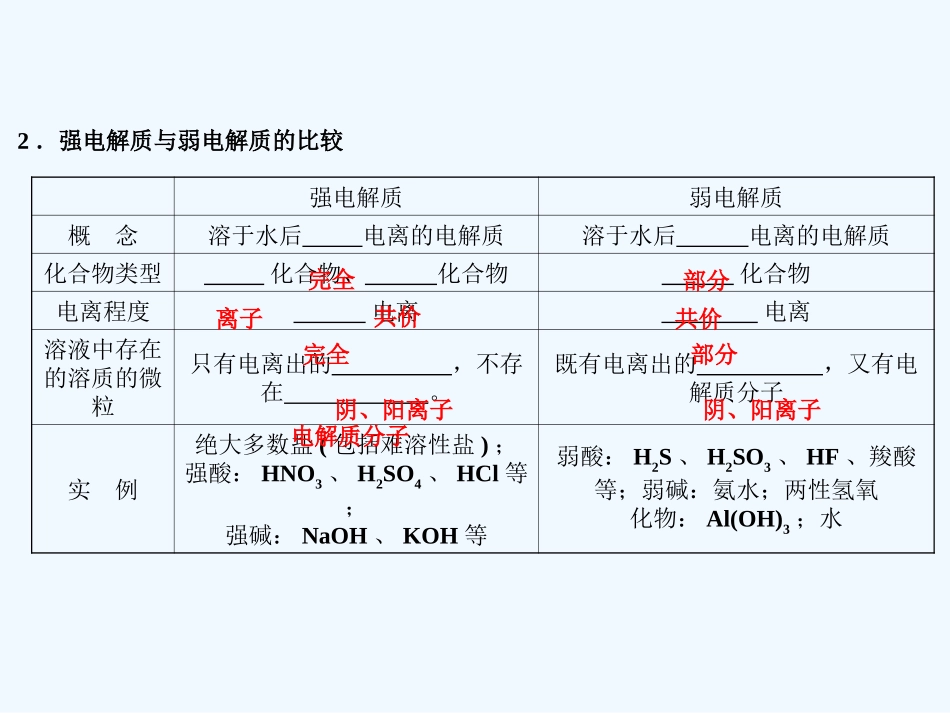
水溶液里或熔融状态化合物水溶液和熔融状态强电解质弱电解质概念溶于水后电离的电解质溶于水后电离的电解质化合物类型化合物、化合物化合物电离程度电离电离溶液中存在的溶质的微粒只有电离出的,不存在
既有电离出的,又有电解质分子实例绝大多数盐(包括难溶性盐);强酸:HNO3、H2SO4、HCl等;强碱:NaOH、KOH等弱酸:H2S、H2SO3、HF、羧酸等;弱碱:氨水;两性氢氧化物:Al(OH)3;水2.强电解质与弱电解质的比较完全离子共价完全阴、阳离子电解质分子部分共价部分阴、阳离子【想一想】1.CO2溶于水,水溶液能导电,CO2是电解质吗
答:判断化合物是不是电解质,溶液的导电性仅仅是一个条件,关键要看是不是化合物本身能够电离出自由移动的离子,CO2的水溶液导电是由于CO2和水化合生成的H2CO3电离出自由移动的离子,而不是CO2电离出的,故CO2不是电解质
2.食盐晶体不导电,那么氯化钠是电解质吗
答:食盐(氯化钠)是由钠离子和氯离子构成的化合物,在固态时不导电,但在水溶液中或熔融状态下能导电,所以氯化钠是电解质,判断时应根据电解质的概念
1.离子反应是指,主要包括和的氧化还原反应
2.离子方程式是用来表示离子反应的式子,书写的具体步骤是“一写”、“二改”、“三删”、“四查”,与化学方程式相比较,离子方程式可表示反应
例如:H++OH-===H2O,就表示强酸和强碱反应生成可溶性盐和水的反应
有离子参加的反应复分解反