第2课时氨和铵盐1
了解氨气、铵盐的性质及用途
2.掌握氨气的实验室制法
3.掌握铵根离子的检验
1.氨的性质(1)氨的物理性质纯净的氨气是色、有的气体,密度比空气
氨很容易液氨气化时要(吸收、放出)大量的热,所以液氨常用作致冷剂
常温常压下,1体积的水可溶解体积的氨气
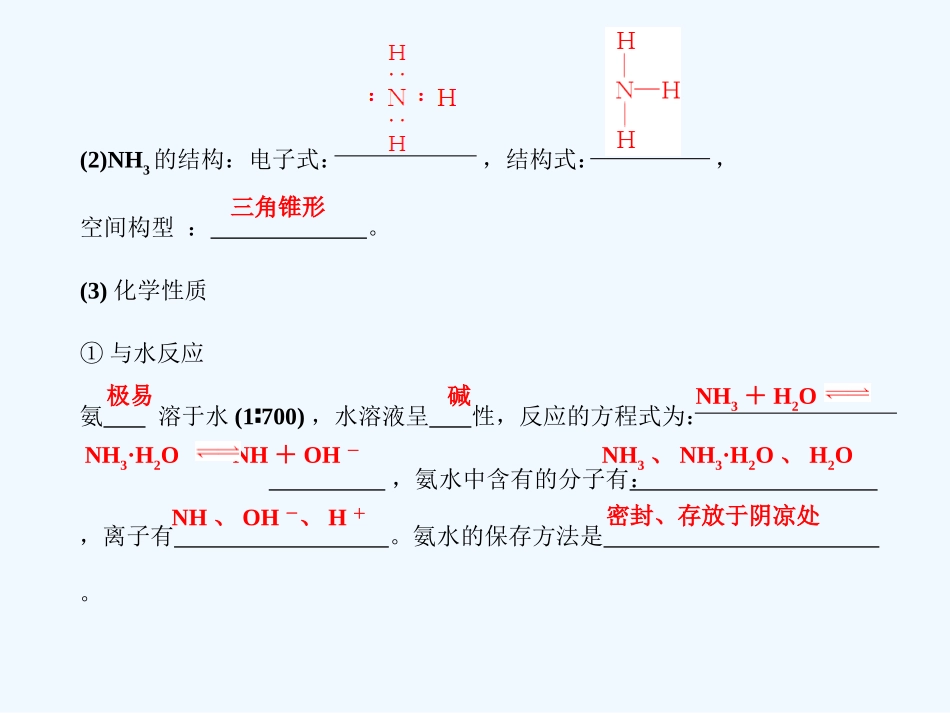
无刺激性气味小液化吸收700(2)NH3的结构:电子式:,结构式:,空间构型:
(3)化学性质①与水反应氨溶于水(1∶700),水溶液呈性,反应的方程式为:,氨水中含有的分子有:,离子有
氨水的保存方法是
三角锥形极易碱NH3+H2ONH3·H2ONH+OH-NH3、NH3·H2O、H2ONH、OH-、H+密封、存放于阴凉处②——与酸反应碱性将蘸有浓氨水的玻璃棒和蘸有浓盐酸的玻璃棒靠近,现象
化学方程式为;写出NH3和HNO3、H2SO4反应的化学方程式:、
③——与氧气反应还原性NH3和O2在催化剂存在下发生的化学反应为:,此反应中的氧化剂是、氧化产物是,电子转移的数目是
产生白烟NH3+HCl===NH4ClNH3+HNO3===NH4NO32NH3+H2SO4===(NH4)2SO46H2O4NH3+5O24NO+O2NO202.铵盐(1)概念铵根离子与酸根离子构成的化合物
(2)NH的结构①NH的电子式为,结构式为,空间构型为
②铵盐中存在的化学键类型有和
正四面体共价键离子键(3)物理性质铵盐都是色晶体,均易溶于水
(4)化学性质①受热易分解:NH4Cl,(NH4)2CO3
②与碱反应:a
+OH-NH3↑+H2Ob.在稀溶液中不加热:+OH-===NH3·H2Oc.在浓溶液中不加热:+OH-===NH3↑+H2O③水解反应:+H2ONH3·H2O+H+NH3↑+HCl↑2NH3↑+CO2↑+H2O↑白思考:如何干燥氨气
提示:氨气为一种碱性气体,应用碱性或中性干燥剂进行干燥,但是无水