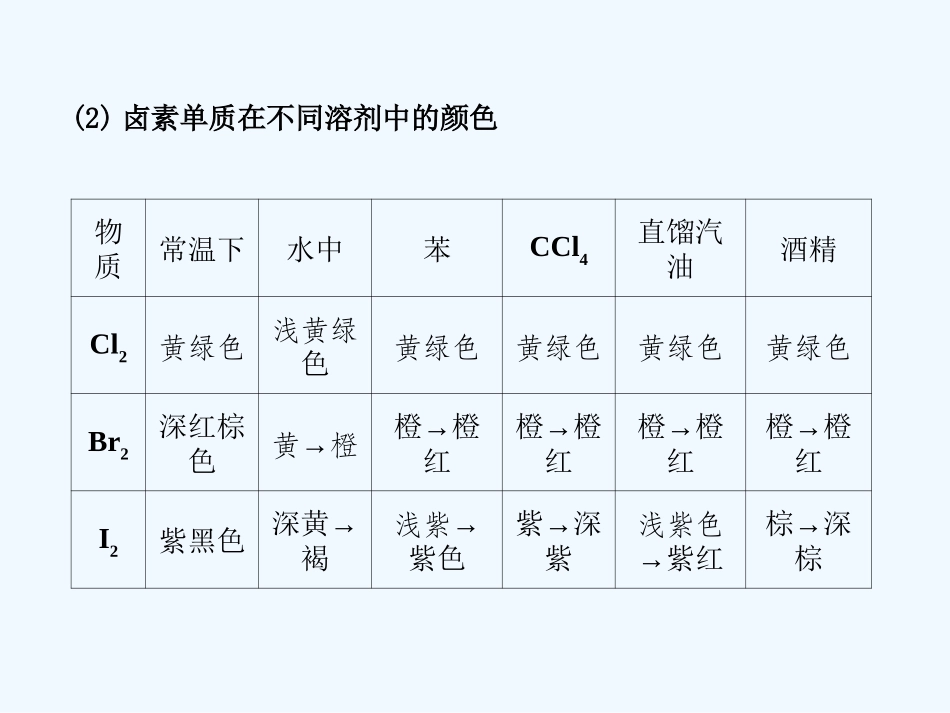
知识点1卤素单质的性质及重要的卤素化合物1.卤素单质的物理性质(1)卤素单质的物理性质及变化规律F2C2Br2I2颜色浅黄绿色黄绿色色色水中溶解度(反应)→逐渐熔、沸点→逐渐状态气态气态态固态深红棕紫黑减小升高液第二节卤族元素(2)卤素单质在不同溶剂中的颜色物质常温下水中苯CCl4直馏汽油酒精Cl2黄绿色浅黄绿色黄绿色黄绿色黄绿色黄绿色Br2深红棕色→黄橙→橙橙红→橙橙红→橙橙红→橙橙红I2紫黑色→深黄褐→浅紫紫色→紫深紫浅紫色→紫红→棕深棕2
卤素单质的化学性质问题2:有哪些重要的卤素化合物
3.几种重要的卤素化合物萤石主要成分为CaF2,不溶于水,白色粉末状固体,是制备HF的主要原料CaF2+H2SO4(浓)===CaSO4+2HF↑氟化氢和氢氟酸氟化氢为极性共价分子,通常情况下为无色气体,在空气中易形成,有毒,溶解于水,其水溶液为氢氟酸;氢氟酸为酸,它可以腐蚀,反应如下:SiO2+4HFSiF4↑+2H2O,因此氢氟酸应保存在铅皿或瓶中,不能在玻璃瓶中存放
氟化物具有较特殊的溶解规律,如AgF易溶,而CaF2难溶氯化钙无水氯化钙具有吸湿性,是常用的中性干燥剂酸雾极易弱玻璃塑料卤化银AgCl、AgBr、AgI均具有感光性,即在光照下分解成黑色的银粒和卤素单质,2AgX2Ag+X2,溴化银用于照相的感光片
碘化银用于人工降雨氯酸钾通常用于实验室制备氧气,具有强氧化性,受撞击容易发生爆炸碘酸钾加碘盐的配料,受热时易分解思维延伸(1)从F→I,气态氢化物的稳定性逐渐减弱,还原性增强;氢化物水溶液的酸性逐渐增强
(2)F2与水反应容易且剧烈,因而F2不能从水溶液中置换出其他卤素单质
知识点2卤素的相似性、递变性、特殊性问题3:卤素的相似性、递变性、特殊性之间有何关系
4.代表性连接着相似性氯的代表性中包含了卤素的相似性,掌握了氯及其化合物的性质,就能推出其他卤素及基化