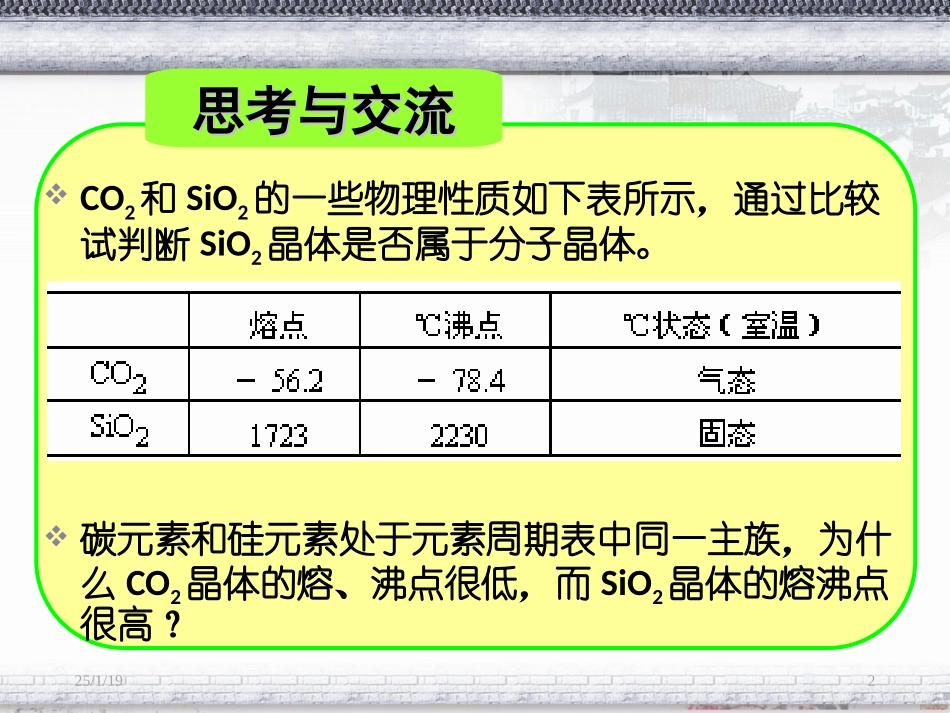
25/1/191第三章晶体结构与性质第二节分子晶体与原子晶体第2课时选修3物质结构与性质25/1/192思考与交流思考与交流CO2和SiO2的一些物理性质如下表所示,通过比较试判断SiO2晶体是否属于分子晶体
碳元素和硅元素处于元素周期表中同一主族,为什么CO2晶体的熔、沸点很低,而SiO2晶体的熔沸点很高
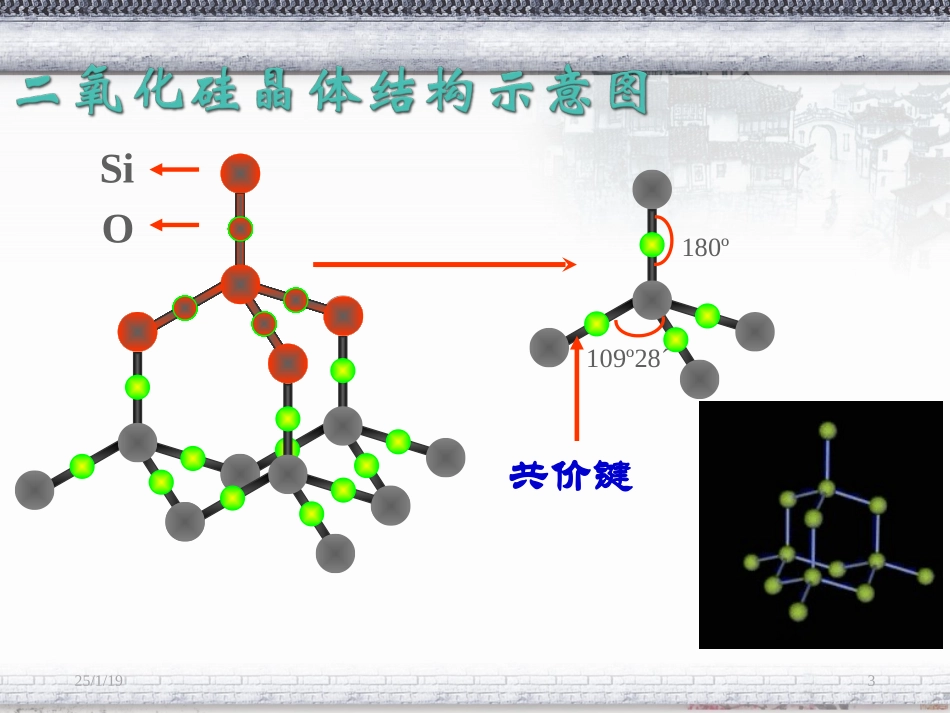
25/1/193180º109º28´SiO共价键25/1/194二、原子晶体注:(1)构成原子晶体的粒子是原子,(2)原子间以较强的共价键相结合
(3)整块晶体是一个三维的共价键网状结构,是一个“巨分子”,又称共价晶体
思考:只由原子形成的晶体一定是原子晶体吗
1、概念:所有的相邻原子间都以共价键相结合而形成空间立体网状结构的晶体
原子晶体25/1/195SiO2的结构特征在SiO2晶体中①1个Si原子和4个O原子形成4个共价键,每个Si原子周围结合4个O原子;同时,每个O原子跟2个Si原子相结合
实际上,SiO2晶体是由Si原子和O原子按1:2的比例所组成的立体网状的晶体
②最小的碳环是由6个Si原子和6个O原子组成的12元环
③1molSiO2中含4molSi—O键25/1/196晶体类型原子晶体熔、沸点(高低)硬度溶解性导电性2、原子晶体的性质很高很大不溶一般不导电(硅是半导体)某些原子晶体的熔点和硬度原子晶体金刚石氮化硼碳化硅石英硅锗熔点/0C>355030002700171014101211硬度109
025/1/197解释:结构相似的原子晶体,原子半径越小,键长越短,键能越大,晶体熔点越高金刚石>碳化硅>晶体硅交流与研讨1、怎样从原子结构角度理解金刚石、硅和锗的熔点和硬度依次下降
2、“具有共价键的晶体叫做原子晶体”
这种说法对吗
解释:不对,分子晶体中通常也含有共价键,如CO2、O2,某些离子晶体中也含共价键,如NaOH、