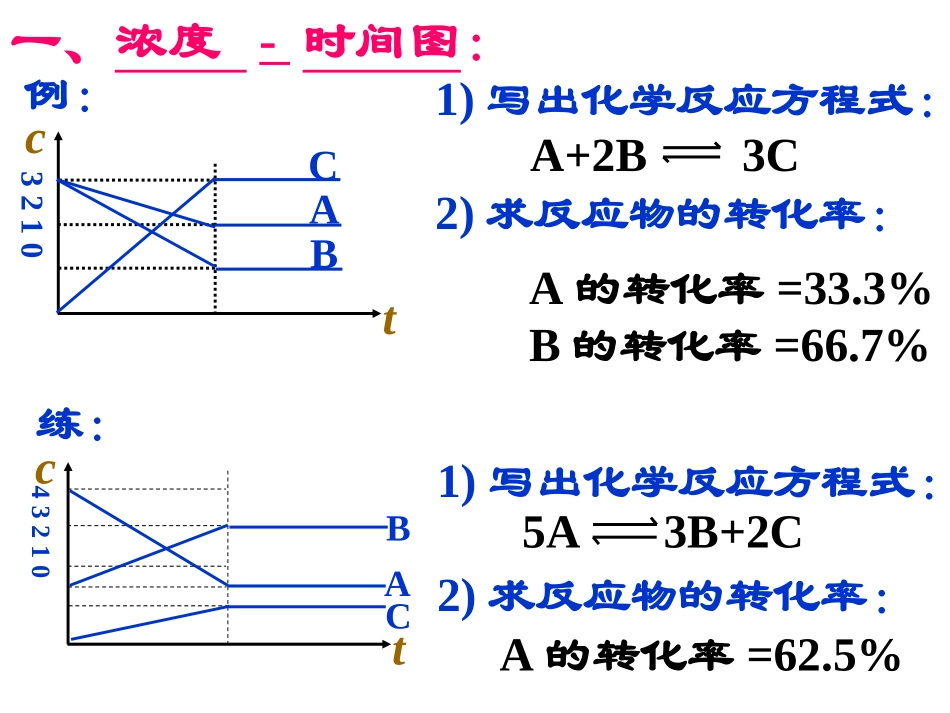
一、浓度-时间图:tcCAB1)写出化学反应方程式:2)求反应物的转化率:A+2B3CABCtc1)写出化学反应方程式:2)求反应物的转化率:例:练:5A3B+2CA的转化率=62
5%321043210A的转化率=33
3%B的转化率=66
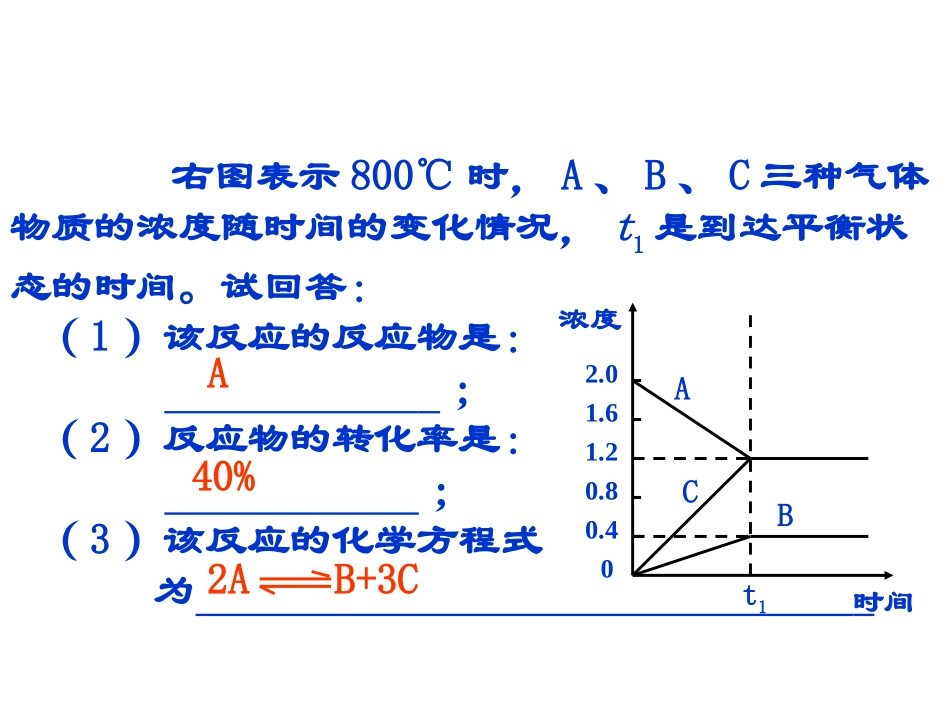
7%A40%右图表示800℃时,A、B、C三种气体物质的浓度随时间的变化情况,t1是到达平衡状态的时间
试回答:(1)该反应的反应物是:;(2)反应物的转化率是:;(3)该反应的化学方程式为2AB+3C浓度时间t100
0ACB可逆反应H2(g)+I2(g)2HI(g)在一定的条件下反应混合物中各组分的浓度(mol·L-1)与时间t(min)的变化曲线如图所示,根据图示,回答(1)时间t1的意义是
(2)在时间0至t1的间隔里,v(I2)=
(3)此平衡状态下,H2的转化率为
达到平衡所用的时间0
2/t1mol·L-1·min-150%二、速度-时间图:可用于:1)(已知反应)判断引起平衡移动的因素
2)已知引起平衡移动的因素,判断反应是吸热或放热,反应前后气体体积的变化
tvv正v逆t1t2•引起平衡移动的因素是,平衡将向方向移动
增大反应物浓度正tvv正v逆t1t2•引起平衡移动的因素是,平衡将向方向移动
减小生成物浓度正•已知对某一平衡改变温度时有如下图变化,则温度的变化是(升高或降低),平衡向反应方向移动,正反应是热反应
t1t2tvv正v逆升高正吸•若对一正反应吸热的可逆反应平衡后降低温度,画出平衡移动过程中的v-t图
t1t2tvv逆v正•对于mA(g)+nB(g)pC(g)+qD(g),改变压强时有如下图变化,则压强变化是(增大或减小),平衡向反应方向移动,m+n(>、p+qD.m+n