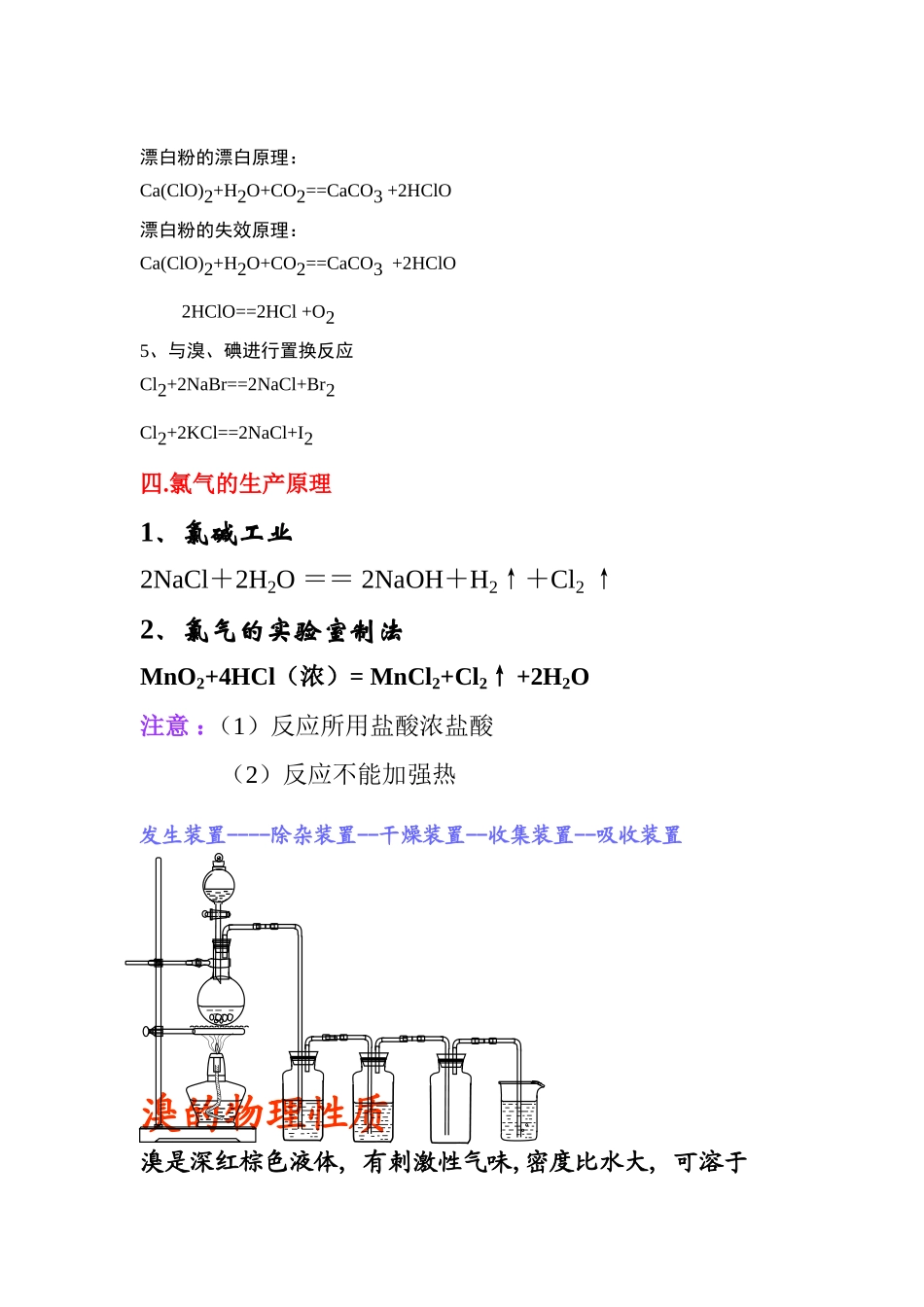
化学必修一复习资料氧化还原反应还原剂-失电子-化合价升高-氧化反应(产物)(还原性)被氧化<生成氧化产物>氧化剂-得电子-化合价降低-还原反应(产物)(氧化性)被还原<生成还原产物>口诀:还原剂--升,失,氧氧化剂--降,得,还。氧化性:氧化剂>氧化产物还原性:还原剂>还原产物卤族元素一、氯气的物理性质氯气是一种黄绿色,有特殊气味的气体,密度比空气大,能溶于水,1体积水可溶解2体积氯气,有剧毒。易液化:钢瓶储存二、氯气的化学性质1.与金属反应1)氯气和金属钠反应:2Na+Cl2===2NaCl剧烈燃烧,生成白烟(2)氯气和铁丝的反应2Fe+3Cl2===2FeCl3剧烈燃烧,生成棕褐色的烟氯气和氢气的反应H2+Cl2===2HCl纯净的氢气在氯气中安静地燃烧,发出苍白色火焰,集气瓶口有白雾,是盐酸的酸雾H2+Cl2===2HCl氢气和氯气的混合气体在光照的条件下,发生爆炸3、与水反应Cl2+H2OHCl+HClO加热或光照2HClO===2HCl+O2↑久制氯水的成分:Cl-,H+,H2OFeCl2溶液溶液颜色由浅绿色变成黄色紫色石蕊试液溶液先变红后褪色AgNO3溶液产生白色沉淀Na2CO3溶液产生气体加有酚酞的NaOH溶液褪色4、与碱反应Cl2+2NaOH==NaCl+NaClO+H2O(用于实验中尾气的吸收)2Cl2+2Ca(OH)2==CaCl2+Ca(ClO)2+2H2O(工业上制取漂白粉)漂白粉的主要成分为:CaCl2和Ca(ClO)2有效成分为:Ca(ClO)2新制氯水的成分:Cl-,H+,ClO-,H2O,HCl,HCIO漂白粉的漂白原理:Ca(ClO)2+H2O+CO2==CaCO3+2HClO漂白粉的失效原理:Ca(ClO)2+H2O+CO2==CaCO3+2HClO2HClO==2HCl+O25、与溴、碘进行置换反应Cl2+2NaBr==2NaCl+Br2Cl2+2KCl==2NaCl+I2四.氯气的生产原理1、氯碱工业2NaCl+2H2O==2NaOH+H2↑+Cl2↑2、氯气的实验室制法MnO2+4HCl(浓)=MnCl2+Cl2↑+2H2O注意:(1)反应所用盐酸浓盐酸(2)反应不能加强热发生装置----除杂装置--干燥装置--收集装置--吸收装置溴的物理性质溴是深红棕色液体,有刺激性气味,密度比水大,可溶于溴水呈橙色.在水中的溶解度不大,易挥发(保存用水封)溴的蒸气红棕色碘的物理性质碘是一种紫黑色固体,具升华性质,碘水呈褐色碘的蒸气呈紫色,密度大于水的固体,在水中溶解度不大。(1)卤素单质化学性质相似,都是活泼的非金属单质;(2)从氟到碘活泼性逐渐减弱;(3)氟与碘有特性。溴、碘单质的化学性质1、相互置换Cl2+2NaBr==2NaCl+Br2Cl2+2Kl==2NaCl+I2Br2+2Kl==2NaBr+I2氧化性:F2>Cl2>Br2>I22、与水的反应(参加反应的极少)Br2+H2O==HBr+HBrOI2+H2O==HI+HIO3、与碱的反应Br2+2NaOH==NaBr+NaBrO+H2OI2+2NaOH==NaI+NaIO+H2O4、Br-、I-的检验—加稀HNO3+硝酸银溶液NaBr+AgNO3==NaNO3+AgBr↓淡黄色KI+AgNO3==KNO3+AgI↓黄色NaCl+AgNO3==NaNO3+AgCl↓白色溴化银的感光性2AgBr===2Ag+Br2碘化银:人工降雨剂工业提取Br2:提取粗盐后的母液→通入Cl2→鼓入热空气→挥发Br2蒸气→冷凝得液溴工业提取I2:海带粉碎→加水浸泡→通入Cl2→过滤→蒸发→升华→冷凝I2蒸气得晶体氟:(1)氟与水反应生成O2:2F2+2H2O=4HF+O2(2)可与惰性气体反应生成XeF2、XeF4、XeF6等.即F无正价(另CaCl2易溶,而CaF2难溶;AgCl难溶,而AgF易溶。)3.实验室洗刷仪器时,对做过碘升华实验的烧杯壁上残留的碘,可用酒精洗涤;对制取氯气用的烧瓶底部沾有的二氧化锰固体,可用浓盐酸洗涤;对玻璃仪器上沾有的铁锈,应用稀盐酸洗涤。正确书写离子反应方程式1、写出化学方程式2、把易溶于水、易电离的物质写成离子形式,难溶或难电离的物质以及气体等仍用化学式表示。3、删去方程式两边形式相同的离子4、整理方程式并检查两边各元素的原子个数和电荷总数是否相等小结:写、拆、删、查2、附加隐含条件的应用规律:⑴溶液无色透明时,则溶液中一定没有色离子。常见的有色离子:Cu2+、Fe3+、Fe2+、MnO4-等⑵强碱性溶液中肯定不存在与OH-反应的离子。⑶强酸性溶液中肯定不存在与H+反应的离子。氧化铝的性质Al2O3+6HCl=2AlCl3+3H2OAl2O3+2NaOH=2NaAlO2+H2O实验室制Al(OH)3AlCl3+3NH3·H2O=Al(OH)3↓+3NH4Cl铝三角(1)Al3++3OH-=Al(OH)3↓(2)Al(OH)3+OH-=AlO2-+2H2O(3)Al3++4OH-=AlO2-+2H2O(4)AlO2-+H++H2O=Al(OH)3↓(5)Al(OH)3+3H+=Al3++3H2O(6)AlO2-+4H+=Al3++2...