2013 年高考化学一轮复习教学教案:2
2《分子的立体构型》第 2 课时(人教版选修 3)学习目标:1
认识杂化轨道理论的要点;2
进一步了解有机化合物中碳的成键特征;3
能根据杂化轨道理论判断简单分子或离子的构型
导学提纲:1
(自学、讨论)鲍林提出杂化轨道理论的目的是什么
什么是杂化轨道
提出杂化轨道理论的目的:合理解释分子的空间构型
在形成多原子分子的过程中,中心原子的若干能量相近的原子轨道重新组合,形成一组新的轨道,这个过程叫做轨道的杂化,产生的新轨道叫杂化轨道
(自学、讨论)甲烷分子的轨道是如何形成的
(思考、讨论)阅读教材 P39~40,并查阅相关资料,请思考:轨道进行杂化时,轨道的数量、能量、以及在空间的分布(形状)是否发生了变化
如果变化,又是如何改变的
请分别以 sp、sp2、sp3杂化轨道为例说明
轨道进行杂化时,轨道的数量没有发生改变,但轨道的能量、以及在空间的分布(形状)均发生了变化
sp 杂化:同一原子中 ns-np 杂化成新轨道:一个 s 轨道和一个 p 轨道杂化组合成两个新的 sp 杂化轨道
杂化轨道间的夹角为 180°,分子的几何构型为直线形
sp2杂化:同一个原子的一个 ns 轨道与两个 np 轨道进行杂化组合为 3 个 sp2 杂化轨道
杂化轨道间的夹角为 120°,分子的几何构型为平面正三角形
sp3杂化:1 个 s 轨道和 3 个 p 轨道会发生混杂,得到 4 个相同的 sp3杂化轨道
杂化轨道间的夹角为 109°28′,分子的空间正四面体或 V 型、三角锥型
(思考、讨论)怎样判断有几个轨道参与了杂化
中心原子杂化 轨道的类型与价层电子对互斥理论(VSEPR)中的“价 层电子对”有何对应关系
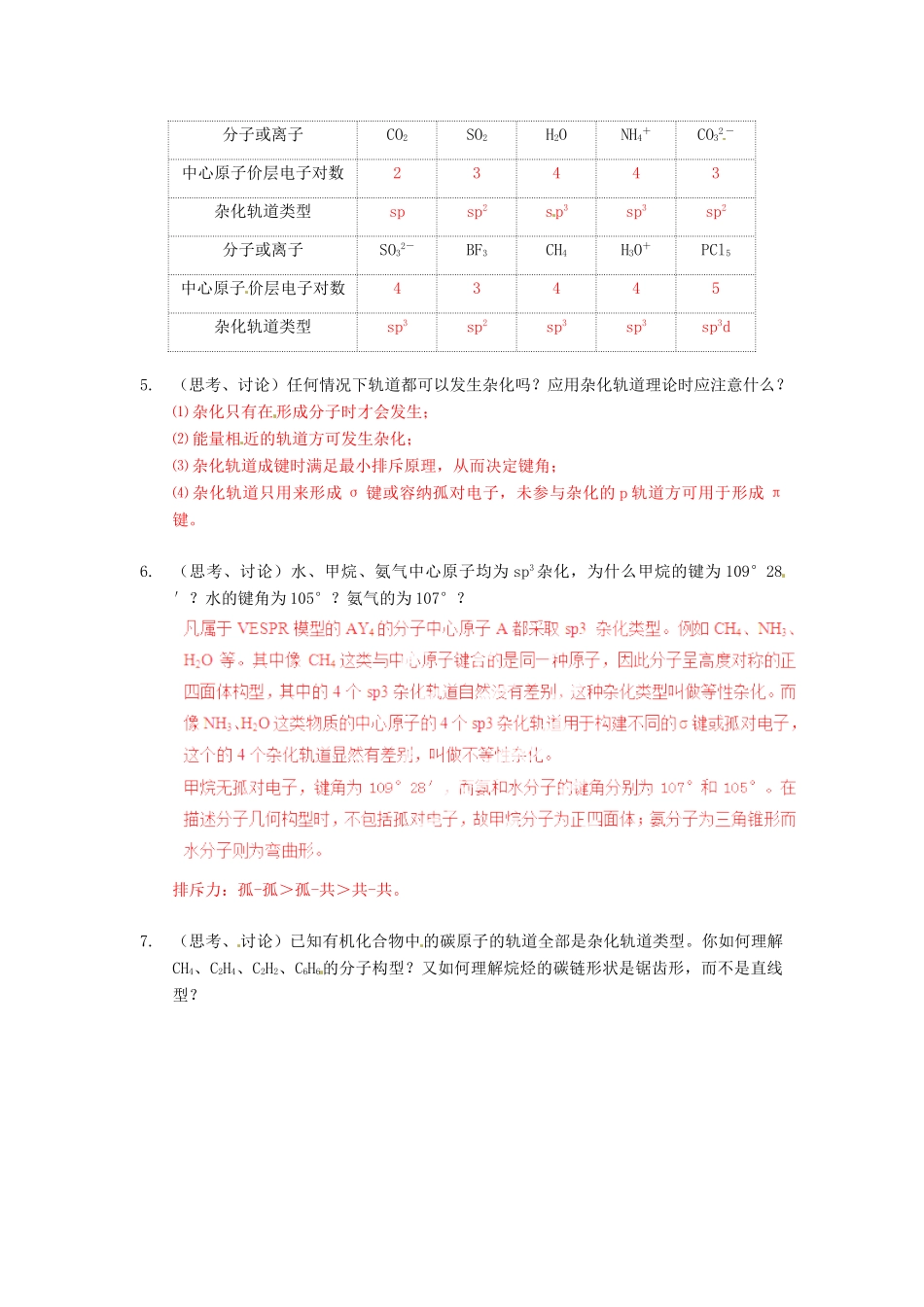
中心原子上的价层电子对为 2、3、4、5、6 时,该中心原子形成的分别是什么样的杂化轨道
中心原子的孤电子对数与相连的其他原子数