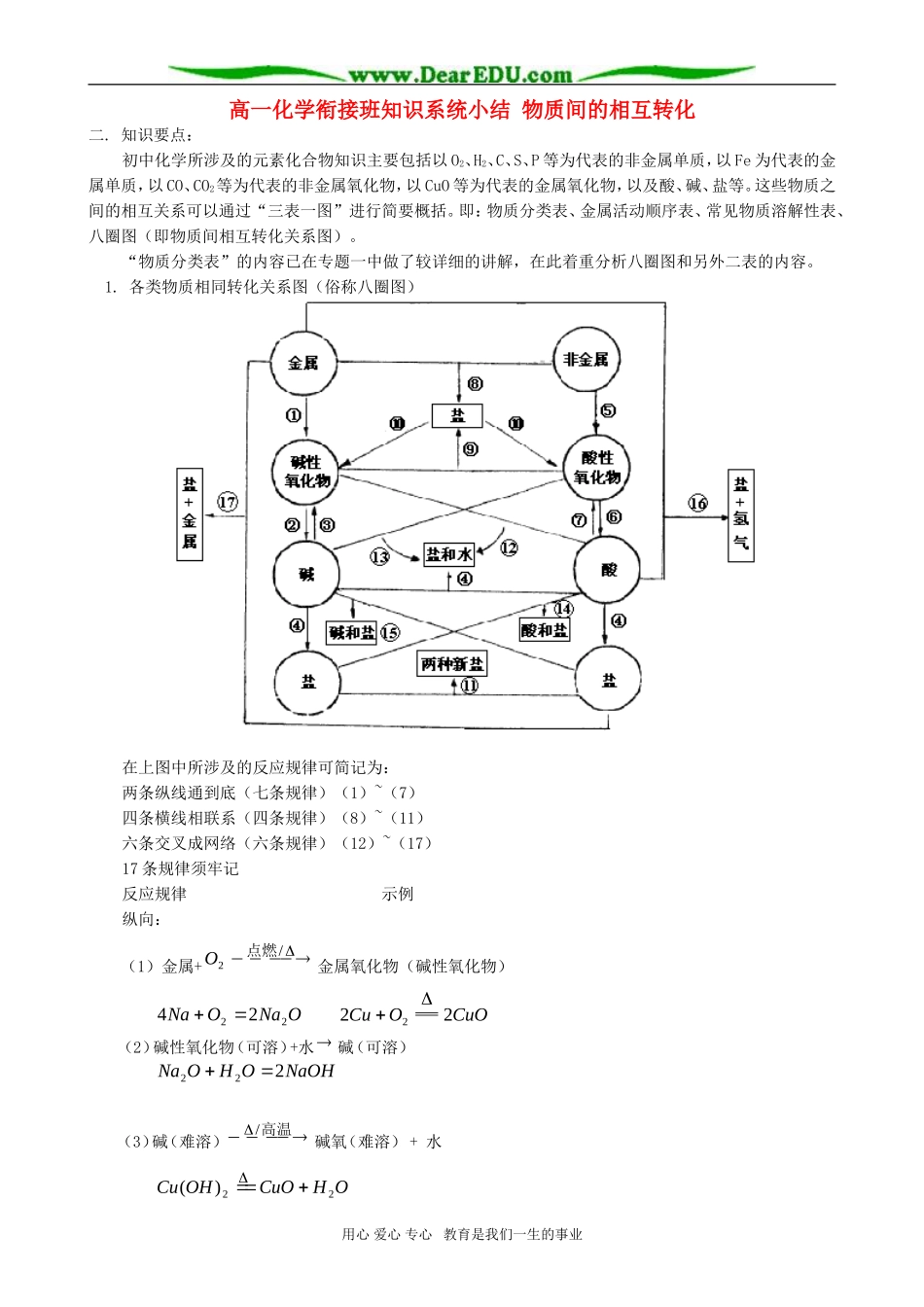
高一化学衔接班知识系统小结物质间的相互转化二.知识要点:初中化学所涉及的元素化合物知识主要包括以O2、H2、C、S、P等为代表的非金属单质,以Fe为代表的金属单质,以CO、CO2等为代表的非金属氧化物,以CuO等为代表的金属氧化物,以及酸、碱、盐等。这些物质之间的相互关系可以通过“三表一图”进行简要概括。即:物质分类表、金属活动顺序表、常见物质溶解性表、八圈图(即物质间相互转化关系图)。“物质分类表”的内容已在专题一中做了较详细的讲解,在此着重分析八圈图和另外二表的内容。1.各类物质相同转化关系图(俗称八圈图)在上图中所涉及的反应规律可简记为:两条纵线通到底(七条规律)(1)~(7)四条横线相联系(四条规律)(8)~(11)六条交叉成网络(六条规律)(12)~(17)17条规律须牢记反应规律示例纵向:(1)金属+/2点燃O金属氧化物(碱性氧化物)ONaONa2224CuOOCu222(2)碱性氧化物(可溶)+水碱(可溶)NaOHOHONa222(3)碱(难溶)高温/碱氧(难溶)+水2)(OHCuOHCuO2用心爱心专心教育是我们一生的事业(4)酸+碱盐+水OHPONaPOHNaOH2434333OHCuSOSOHOHCu244222)((5)非金属+点燃2O非金属氧化物(酸性氧化物)22COOC点燃522254OPOP点燃(6)酸性氧化物(易溶)+水酸(易溶)3222COHOHCO4325223POHOHOP(7)酸(易挥发/难溶)酸氧+水(易挥发/难溶)2232COOHCOH2232SiOOHSiOH从纵向来看,金属碱性氧化物碱盐,其中金属元素相同。非金属酸性氧化物酸(含氧酸)盐,其中非金属元素相同。横向:(8)金属+非金属(无氧酸)盐NaClClNa222点燃(9)碱氧+酸氧(含氧酸)盐32CaSiOSiOCaO高温(10)含氧酸盐碱氧+酸氧23COCaOCaCO高温(11)盐+盐两种新盐AgClNaNOAgNONaCl33交叉:(12)酸+碱氧盐+水OHCuSOCuOSOH2442(13)碱+酸氧盐+水OHCONaCONaOH23222(14)酸+盐新酸+新盐32423242COHSONaCONaSOH2232COOHCOH(15)碱+盐新碱+新盐用心爱心专心教育是我们一生的事业2424)(2OHCuSONaCuSONaOH(16)金属+酸盐+2H2442)(HZnSOSOHZn稀(17)金属+盐新盐+新金属44ZnSOCuCuSOZn以上十七条规律的应用:(1)可知某物质的性质。(2)可知某物质的制法。如:(4)、(8)、(9)、(11)~(17)为盐的十种制法。(3)已知各类物质间的相互关系。说明:<1>以上各规律为各物质间相互转化的一般规律,具体到某些物质有些规律要具体分析,未必均适用。如:制取2ZnCl的方法与制取4CuSO的方法各有几种?(思考)答:制取2ZnCl:①222HZnClHClZn②OHZnClHClZnO222③OHZnClHClOHZn22222)(④22232COOHZnClHClZnCO⑤22ZnClClZn点燃⑥4224BaSOZnClBaClZnSO⑦CuZnClCuClZn22因2ZnCl为无氧酸盐,故规律(9)、(13)不适用。因2)(OHZn为难溶碱,故规律(15)不适用。∴只有如上7种制法。制取4CuSO:①OHCuSOSOHCuO2442②OHCuSOSOHOHCu244222)(用心爱心专心教育是我们一生的事业③224423COOHCuSOSOHCuCO因Cu为H后金属,2)(OHCu为难溶碱、CuO不能直接与SO3反应生成CuSO4,Ag2SO4为微溶物,不符合与CuCl2发生复分解反应的条件,也不能与Cu发生置换反应等原因,∴CuSO4只有上述三种制取方法(初中范围内,方法③也不常见)<2>此外,在物质的制取中还有一些常见的规律,如:对于盐+酸新盐+新酸,有如下规律:①强酸弱酸如:22232COOHCaClHClCaCO②稳定的(不易分解的)酸不稳定的(另分解的)酸。如:22232COOHCaClHClCaCO③高沸点(不易挥发的)酸低沸点(易挥发的)酸。如:HClSONaNaClSOH2)(2)(4242固浓④可溶性酸难溶性酸。如:323222SiOHNaClHClSiONa<3>从反应规律与反应类型的关系来看。属于化合反应的有:规律(1)、(2)、(5)、(6)、(8)、(9)。属于分解反应的有:规律(3)、(7)、(10)。属于置换反应的有:规律(16)、(17)。属于复分解反应...