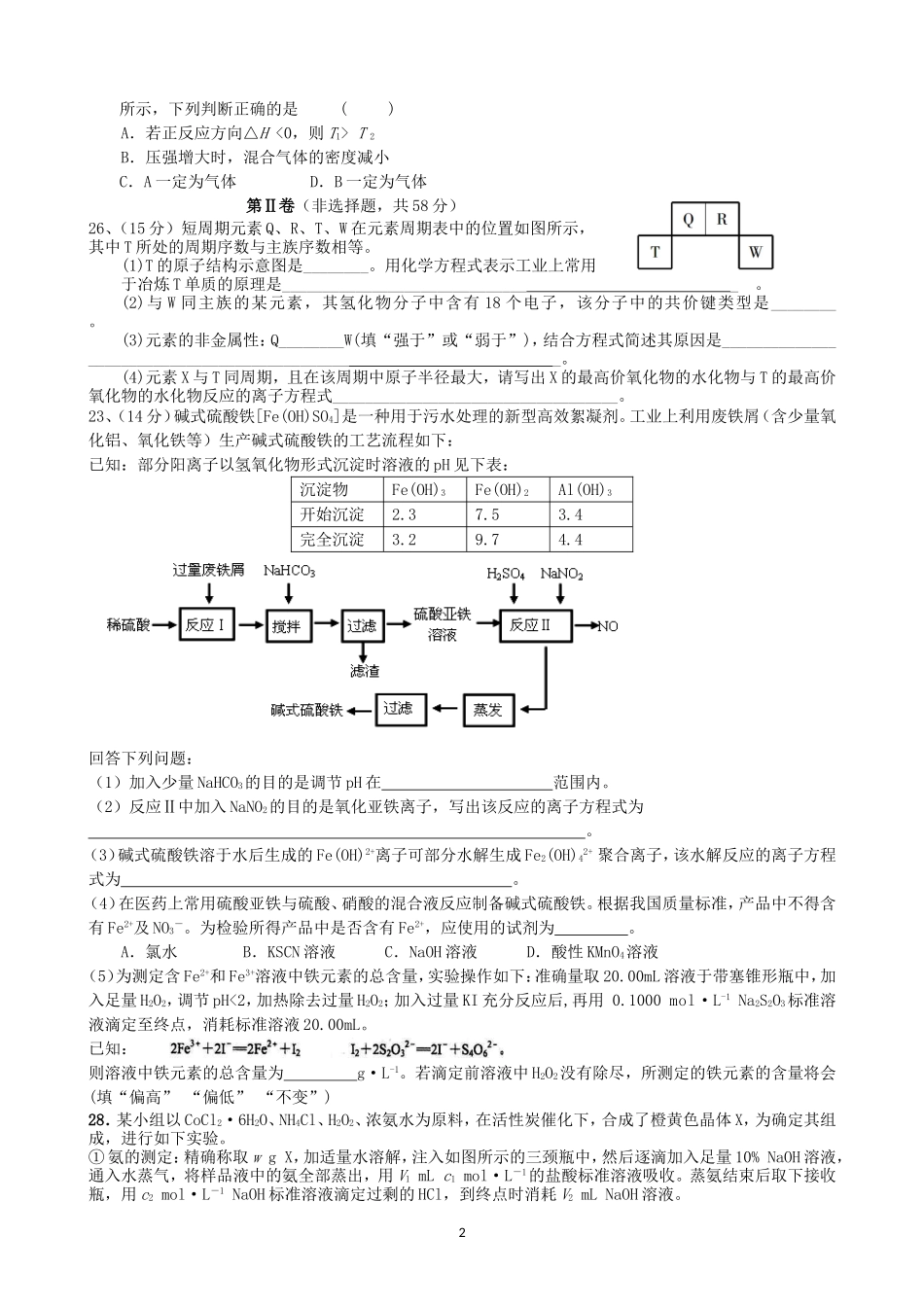
2015化学周考五姓名学号H-1N-14C-12O-16S-32Na-23Al-27Cu-64Fe-56Cl-35.5Ba-137Zn-65P-31第Ⅰ卷一、选择题(每小题只有一个选项符合题目要求,选择题共42分6.化学与生活、社会密切相关。下列说法不正确的是()A.利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境B.用废旧皮革生产药用胶囊可以提高原子利用率C.为防止电池中的重金属等污染土壤和水体,应积极开发废电池的综合利用技术D.提倡人们购物时不用塑料袋,是为了防止白色污染7.下列化学用语描述中不正确的是()A.中子数为20的氯原子:3717ClB.比例模型可以表示CO2分子或SiO2分子C.HCO3的电离方程式为:HCO3+H2OCO23+H3O+D.次氯酸的结构式:H-O-Cl8.用NA表示阿伏加德罗常数的值。下列叙述中正确的是()A.0.1mol—NH2(氨基)中含有的电子数目为1.0NAB.常温下,1L0.1mol·L-1CH3COONa溶液中含有的CH3COO-和Na+总数为0.2NAC.标准状况下,2.24LH2O中含有的原子总数为3NAD.常温常压下,16gO2和O3混合气体含有的氧原子数为NA9.下列表示化学反应的离子方程式,其中正确的是()A.NaAlO2溶液中滴加过量盐酸:AlO2-+H2O+H+=Al(OH)3B.NH4HSO3溶液与足量浓NaOH溶液共热:NH4++HSO3-+2OH-=NH3↑+SO32-+H2OC.明矾溶于水产生Al(OH)3胶体:Al3++3H2OAl(OH)3↓+3H+D.FeCl3溶液与Cu反应:Fe3++Cu=Fe2++Cu2+10.在一无色溶液中检验出有Ba2+、Ag+,同时又测得其酸性很强。某学生还要鉴定此溶液中是否大量存在:①Cu2+②Fe3+③Cl-④NO3-⑤S2-⑥CO32-⑦NH4+⑧Mg2+⑨Al3+⑩AlO2-离子。其实,这些离子中有一部分不必再鉴定就能加以否定,你认为不必鉴定的离子组是()A.③⑤⑥⑦⑩B.①②⑤⑥⑧⑨C.③④⑦⑧⑨D.①②③⑤⑥⑩11.一种新型燃料电池,一极通入空气,另一极通入丁烷气体;电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-。下列说法不正确的是()A.在熔融电解质中,O2-向负极定向移动B.电池的总反应是:2C4H10+13O2===8CO2+10H2OC.通入空气的一极是正极,电极反应为:O2+4e-===2O2-D.通入丁烷的一极是负极,电极反应为:C4H10+26e-+13O2-===4CO2↑+5H2O12.下列溶液中有关物质的浓度关系正确的是()A.c(NH4+)相等的(NH4)2SO4、NH4HSO4、NH4Cl溶液:c(NH4HSO4)>c((NH4)2SO4)>c(NH4Cl)B.等物质的量的NaClO、NaHCO3混合溶液:c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)+c(CO32-)C.向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-)D.某二元弱酸的酸式盐NaHA溶液中:c(H+)+c(Na+)=c(OH-)+c(HA-)+c(A2-)13.在密闭容器中,对于可逆反应A+3B2C(气),平衡时C的体积分数与温度和压强的关系如图12345671C%T1T2p(Pa)所示,下列判断正确的是()A.若正反应方向△H<0,则T1>T2B.压强增大时,混合气体的密度减小C.A一定为气体D.B一定为气体第Ⅱ卷(非选择题,共58分)26、(15分)短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等。(1)T的原子结构示意图是________。用化学方程式表示工业上常用于冶炼T单质的原理是_______________________________。(2)与W同主族的某元素,其氢化物分子中含有18个电子,该分子中的共价键类型是________。(3)元素的非金属性:Q________W(填“强于”或“弱于”),结合方程式简述其原因是_______________________________________________。(4)元素X与T同周期,且在该周期中原子半径最大,请写出X的最高价氧化物的水化物与T的最高价氧化物的水化物反应的离子方程式___________________________________。23、(14分)碱式硫酸铁[Fe(OH)SO4]是一种用于污水处理的新型高效絮凝剂。工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁的工艺流程如下:已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:沉淀物Fe(OH)3Fe(OH)2Al(OH)3开始沉淀2.37.53.4完全沉淀3.29.74.4回答下列问题:(1)加入少量NaHCO3的目的是调节pH在范围内。(2)反应Ⅱ中加入NaNO2的目的是氧化亚铁离子,写出该反应的离子方程式为。(3)碱式...