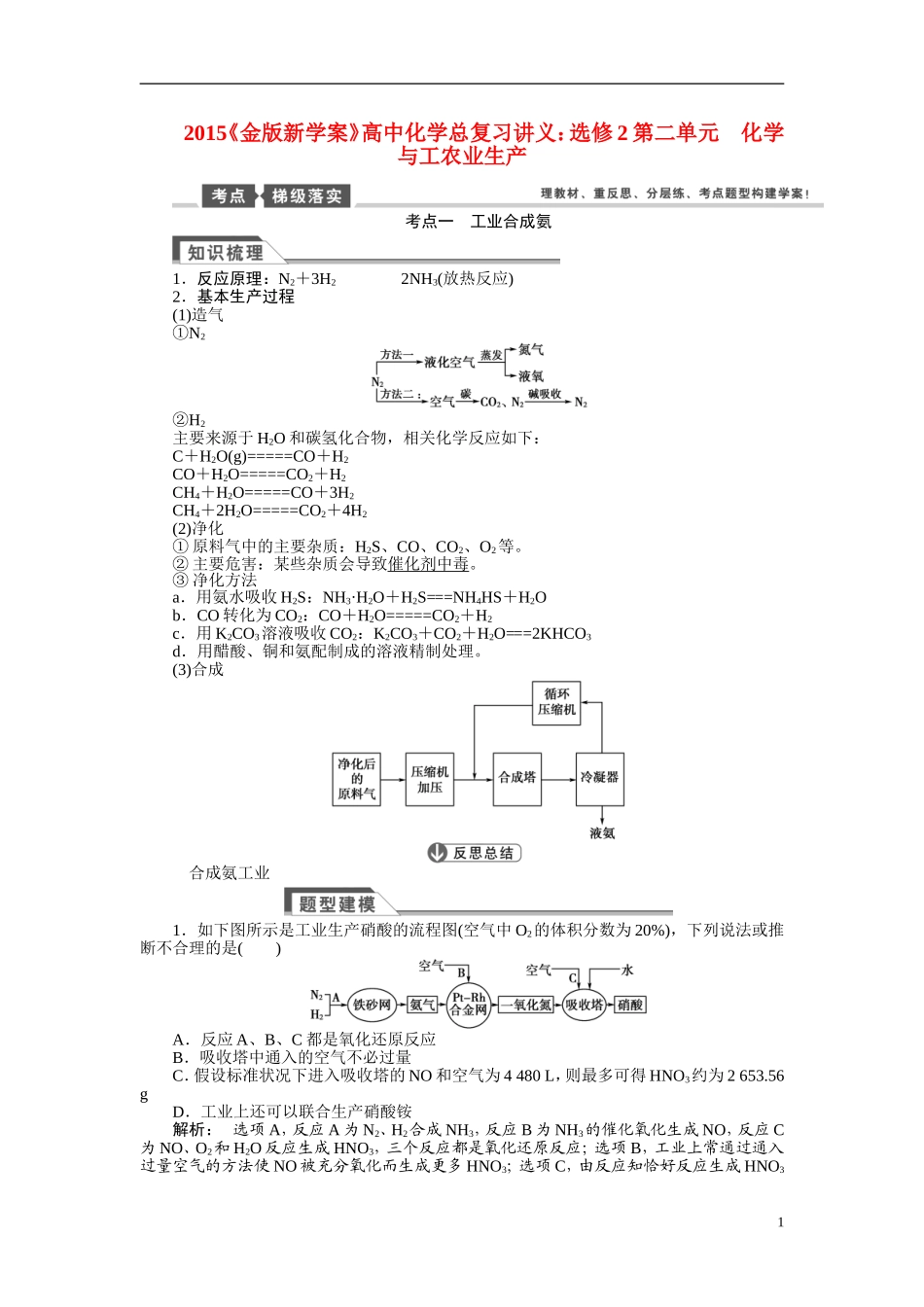
2015《金版新学案》高中化学总复习讲义:选修2第二单元化学与工农业生产考点一工业合成氨1.反应原理:N2+3H22NH3(放热反应)2.基本生产过程(1)造气①N2②H2主要来源于H2O和碳氢化合物,相关化学反应如下:C+H2O(g)=====CO+H2CO+H2O=====CO2+H2CH4+H2O=====CO+3H2CH4+2H2O=====CO2+4H2(2)净化①原料气中的主要杂质:H2S、CO、CO2、O2等
②主要危害:某些杂质会导致催化剂中毒
③净化方法a.用氨水吸收H2S:NH3·H2O+H2S===NH4HS+H2Ob.CO转化为CO2:CO+H2O=====CO2+H2c.用K2CO3溶液吸收CO2:K2CO3+CO2+H2O===2KHCO3d.用醋酸、铜和氨配制成的溶液精制处理
(3)合成合成氨工业1.如下图所示是工业生产硝酸的流程图(空气中O2的体积分数为20%),下列说法或推断不合理的是()A.反应A、B、C都是氧化还原反应B.吸收塔中通入的空气不必过量C.假设标准状况下进入吸收塔的NO和空气为4480L,则最多可得HNO3约为2653
56gD.工业上还可以联合生产硝酸铵解析:选项A,反应A为N2、H2合成NH3,反应B为NH3的催化氧化生成NO,反应C为NO、O2和H2O反应生成HNO3,三个反应都是氧化还原反应;选项B,工业上常通过通入过量空气的方法使NO被充分氧化而生成更多HNO3;选项C,由反应知恰好反应生成HNO31时,NO与O2的体积比为4∶3,设标准状况下4480L中,含有4amolNO,则含有15amol空气,则有:4a+15a=200,则a≈10
53,故最多可得HNO3的质量为4×10
53mol×63g·mol-1=2653
56g;选项D,合成的NH3与HNO3反应可生成NH4NO3
答案:B2.工业合成氨是