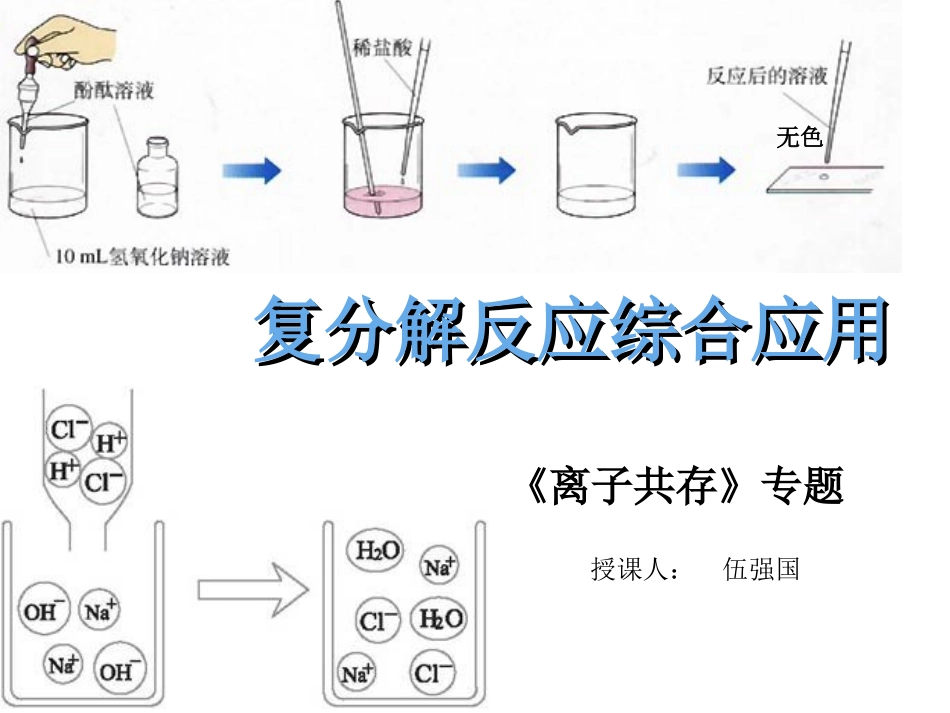
复分解反应综合应用复分解反应综合应用授课人:伍强国无色《离子共存》专题1、下列物质能共存于同一溶液中,且无色透明的是()A.NaOH、NaNO3、K2SO4B.CuSO4、MgSO4、KClC.Ba(OH)2、H2SO4、NaClD.NaCl、AgNO3、HNO32、将下列物质同时加入到pH=14的溶液中,能大量共存且得到无色透明溶液的是()A.NaClKClNaNO3B.KClHCl(NH4)2SO4C.K2CO3Ba(NO3)2NaOHD.FeCl3NaClKNO3AA练一练昨天学的,今天你会做吗
2NaOH+H2SO4=Na2SO4+2H2O(中和反应)2Na++2OH-+2H++SO42-=2Na++SO42-+2H2OOH-+H+=H2ONa2CO3+2HCl=2NaCl+H2O+CO2↑CO32-+H+=H2O+CO2↑2Na++CO32-+2H++2Cl-=2Na++2Cl-+H2O+CO2↑结合上节课所学内容(举例如下),回忆复分解反应的微观实质是什么
回忆:酸、碱、盐的溶液中部分离子发生反应,生成沉淀、气体或H2OCO32-+H+→H2O+CO2↑H++OH-→H2OCO32-+Ca2+→CaCO3↓H++HCO3-→H2O+CO2↑CO32-+Ba2+→BaCO3↓Cl-+Ag+→AgCl↓SO42-+Ba2+→BaSO4↓NH4++OH-→NH3↑+H2OCu2++OH-→Cu(OH)2↓Fe3++OH-→Fe(OH)3↓Mg2++OH-→Mg(OH)2↓离子间不能共存的条件两种离子相互作用如果有气体、水或沉淀生成,则这两种离子不能在同一溶液共存
(蓝色)(红褐色)及所得产物的特征:初中化学阶段常见的不共存离子如下:在溶液中不能共存的:(1)能反应的酸碱盐①生成难溶物或微溶物:如SO42-与Ba2+、Ag+;OH-与Cu2+、Fe3+、Mg2+、Al