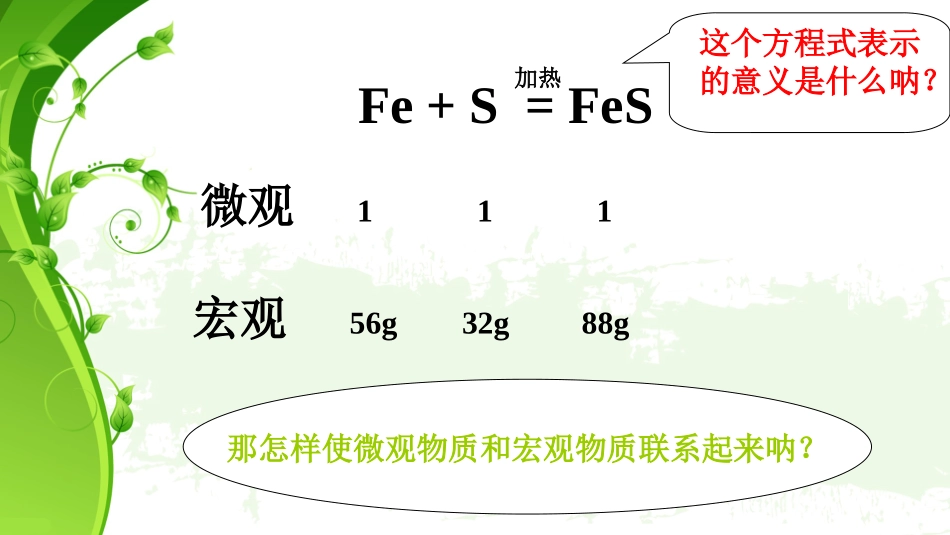
第二节化学计量在实验中的应用Fe+S=FeS加热微观这个方程式表示的意义是什么呐
111宏观56g32g88g那怎样使微观物质和宏观物质联系起来呐
一、物质的量1、含义:国际单位制中的7个基本物理量之一,它表示含有一定数目粒子的集合体,符号为n
2、物质的量的单位:摩尔,简称:摩,符号:mol我们要注意几个问题:1、物质的量这四个字是一个整体,不能简化或增添任何字
2、物质的量计量的对象:微观粒子(分子、原子、离子、原子团、电子、中子、质子等)3、使用物质的量时:表述要确切,指代须明确,一般用:数量+单位+粒子(1molH2、2molSO42-,也可以是1mol氢气)判断这两种说法是否正确:1、2mol氢()2、1mol大米()××2、物质的量的单位——摩尔(mol)标准:1mol粒子集体所含的粒子数与0
012kg12C中所含的碳原子数相同,约为6
02×1023
3、阿伏加德罗常数把1mol任何粒子的粒子数叫做阿伏加德罗常数,通常用6
02×1023mol-1表示,符号为NA
注意:1、碳是12C2、阿伏加德罗常数NA数值≈6
02×10233、阿伏加德罗常数有单位:mol-14、阿伏加德罗常数NA数值=0
012kg12C中所含原子数感受阿伏加德罗常数如果把如果把6
02×106
02×102323个直径为个直径为2
5cm的硬币排成一的硬币排成一行,可以来回于地球与太阳之间行,可以来回于地球与太阳之间240
8亿次亿次如果把如果把6
02×106
02×102323粒米给全球粒米给全球6060亿人吃,每人亿人吃,每人每天吃一斤,要吃每天吃一斤,要吃1414万年,所以物质的量只用来表示万年,所以物质的量只用来表示原子、分子、离子等微观粒子
原子、分子、离子等微观粒子
物质的量、阿伏加德罗常数、粒子数存在怎样的关系呐
NA=N/nn=N/NA①N=N