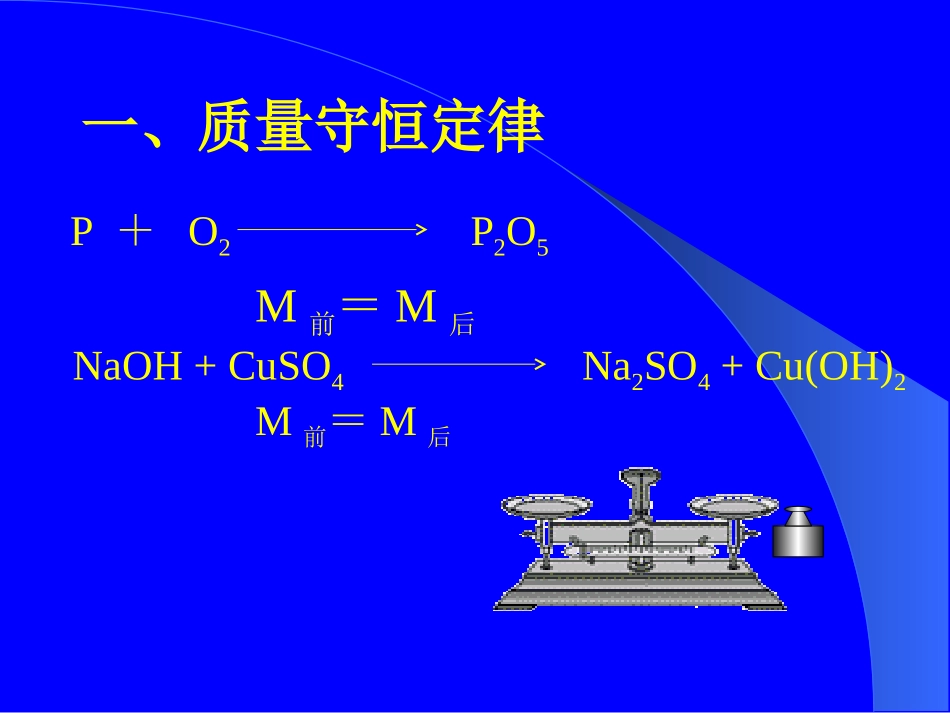
第一节质量守恒定律授课人:陈海霞授课班级:初三、4班一、质量守恒定律M前=M后M前=M后P2O5P+O2Na2SO4+Cu(OH)2NaOH+CuSO4二、质量守恒的原因在一切化学反应中,反应前后:原子的种类、数目、质量都没有变化
故:参加化学反应的各物质的质量总和=生成的各物质的质量总和2、几点说明(1)只适用于化学变化(2)参加(3)生成的(4)总质量(5)“恰好反应”“充分反应”“正好反应”例1:下列说法遵循质量守恒定律的是:()A1g水加热变成1g水蒸气,质量不变,符合质量守恒定理
B在加热氯酸钾和二氧化锰混合物制氧气时,二氧化锰质量在反应前后不变,符合质量守恒定律C高锰酸钾在受热分解后,剩余固体的质量比反应物的质量轻D铁丝在氧气中燃烧后,生成物的质量比原来细铁丝的质量大例2:如图,二分子的甲反应生成二分子的乙与一分子的丙,已知甲乙丙三者为不同的纯净物,则乙物质的化学式为()A:A2B:A2BC:AB2D:A4B2+
±íʾBÔ×Ó±íʾAÔ×Ó甲甲丙丙乙乙例3:将15g的A,10g的B和9g的C三种固体混合物加热充分反应,反应停止后,A剩余3g,B增至25g,C完全消耗,并有新气体D生成,问生成气体D的质量是_____g
例4:17世纪人们认为水能变成土,1769年科学家拉瓦锡对此进行研究
他将一定量的蒸馏水加入特殊的蒸馏器,反复加热101天,发现蒸馏器内产生少量沉淀,称得整个蒸馏器总质量没变,水的质量也没变,沉淀的质量等于蒸馏器减少的质量
对于这项研究说法错误的是()A准确称量是科学研究的重要方法B水在长时间加热后能变成土C物质变化过程中总质量守恒D沉淀物来自蒸馏器本身例5:4
6g某可燃物完全燃烧需9
6g氧气,生成8
8g二氧化碳和5
4g水的事实,可判断某可燃物一定()(填“含”或“不含”)氧元素
例题欣赏☞☞[解析]关键判断可燃物是否含氧元素8