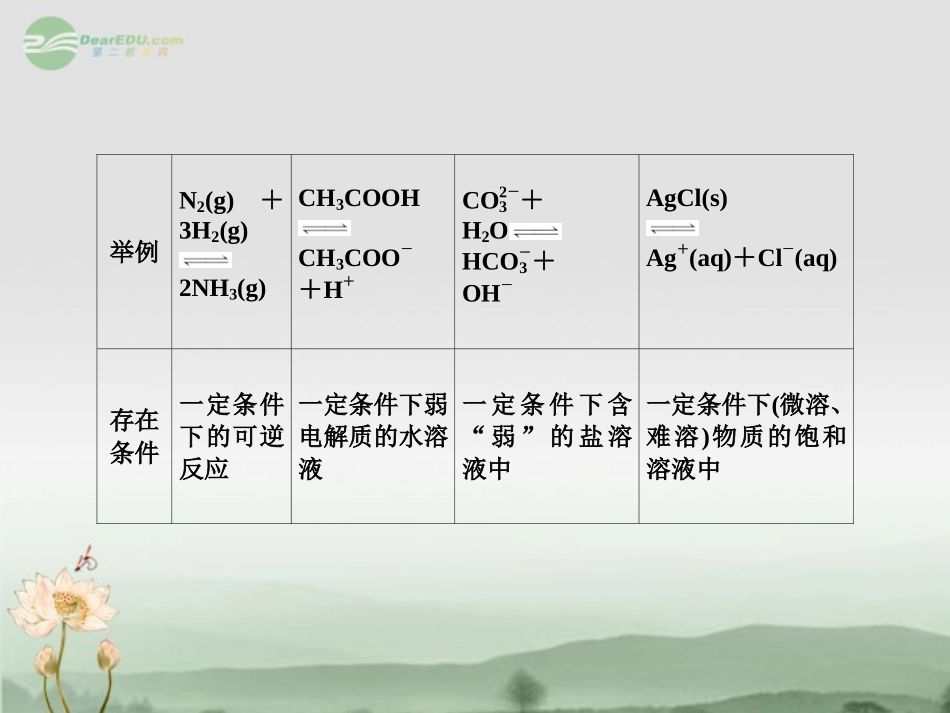
热点专题整合四种重要的动态平衡比较比较项目化学平衡电离平衡水解平衡沉淀溶解平衡平衡特征逆、动、等、定、变v(正)=v(逆)v(电离)=v(结合)v(水解)=v(中和)v(沉淀)=v(溶解)举例N2(g)+3H2(g)2NH3(g)CH3COOHCH3COO-+H+CO2-3+H2OHCO-3+OH-AgCl(s)Ag+(aq)+Cl-(aq)存在条件一定条件下的可逆反应一定条件下弱电解质的水溶液一定条件下含“弱”的盐溶液中一定条件下(微溶、难溶)物质的饱和溶液中影响因素①温度;②浓度;③压强①温度;②浓度;③同离子酸、碱、盐和化学反应①温度;②浓度;③外加电解质和化学反应①温度;②浓度;③酸、碱、盐平衡限度标准K、Ka(Kb)、KW、Ksp影响因素温度平衡移动的判据勒夏特列原理(向减弱条件改变的方向移动)(2012·珠海北大附中检测)A、B、C、D、E五种溶液分别是NaOH、NH3·H2O、CH3COOH、HCl、NH4HSO4中的一种
常温下进行下列实验:①将1LpH=3的A溶液分别与0
001mol·L-1xLB溶液、0
001mol·L-1yLD溶液充分反应至中性,x、y大小关系为:yE③参加反应的锌粉物质的量A=E④反应过程的平均速率E>A⑤A溶液里有锌粉剩余⑥E溶液里有锌粉剩余(4)将等体积、等物质的量浓度B和C混合后溶液,升高温度(溶质不会分解)溶液pH随温度变化如图中的________曲线(填写序号)
(5)室温下,向0
01mol·L-1C溶液中滴加0
01mol·L-1D溶液至中性,得到的溶液中所有离子的物质的量浓度由大到小的顺序为________
【精讲精析】(1)从①可知,A为酸性溶液,则B与D只能为碱性溶液,可能为NaOH、NH3·H2O,当反应达中性后,消耗B溶液的量超过了D溶液,显然这是由于B与酸生成的盐因水解而呈酸性,需要加入稍