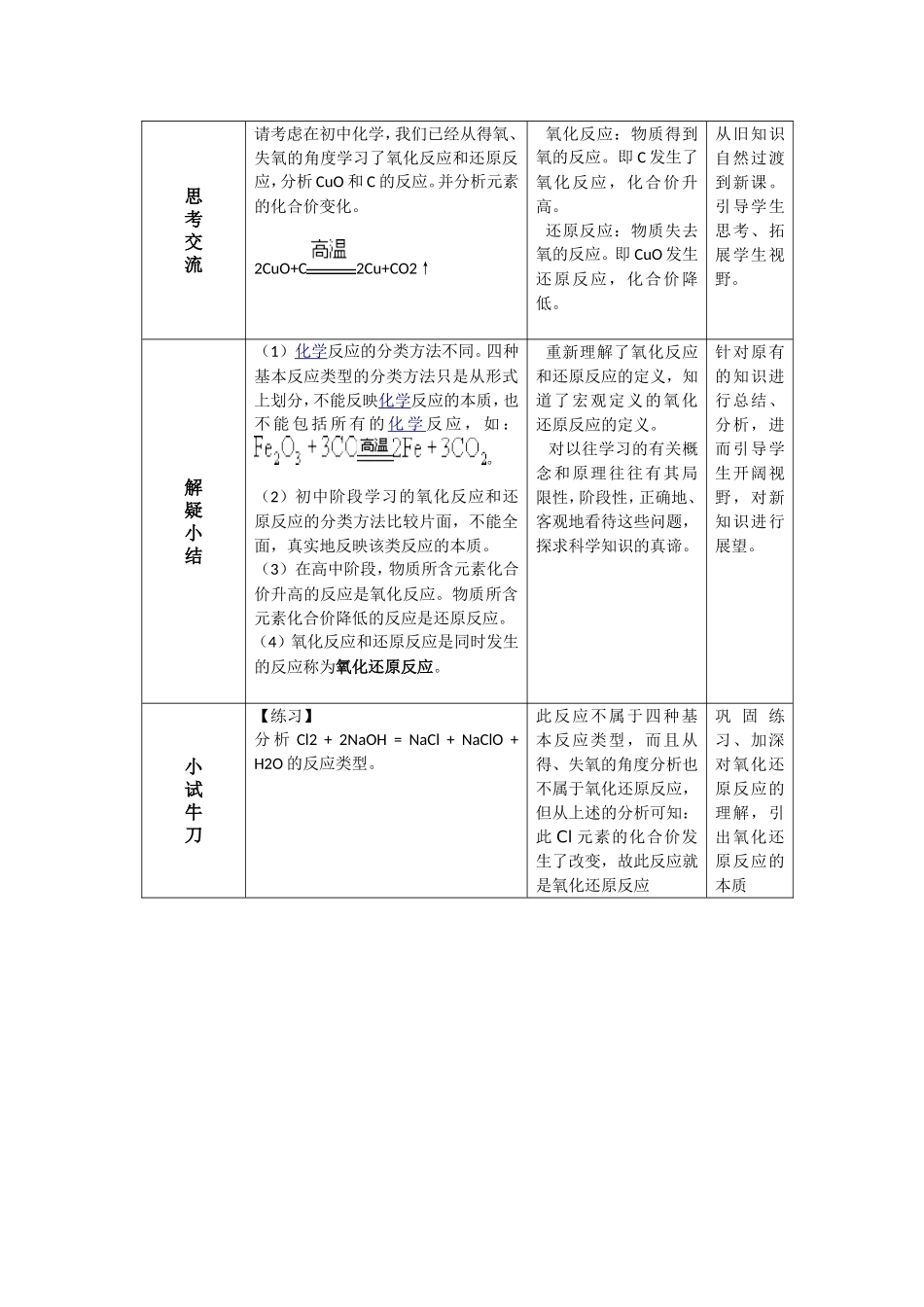
《氧化还原反应》教学设计一、教学起点分析(一)、教学内容分析1、《氧化还原反应》安排在人教版必修《化学1》第二章“化学物质及其变化”第3节
此节内容分两部分,第一部分是介绍氧化还原反应的概念及其本质和特征,第二部分是了解常见的氧化剂和还原剂及氧化还原反应的应用
2、氧化还原反应是日常生活、工农业生产和现代科技中经常遇到的一类重要的化学反应
它贯穿中学化学学习的全过程,是学习中学化学的主线和关键之一
本节教材安排在这里是承前启后,它既复习了初中的基本反应类型及氧化反应、还原反应的重要知识,并以此为铺垫展开对氧化还原反应的较深层次的学习,还将是今后联系元素化合物知识的重要纽带
(二)、学习者分析1、学生在初中化学已经学会通过生成物和反应物的种类和个数判定四种基本反应类型(化合反应、分解反应、复分解反应、置换反应);从具体的反应理解氧化反应和还原反应,但并没认识到氧化还原反应的本质特征;学习了化合价,知道元素周期表前20位元素的主要化合价,理解了化合价的变化,但并没有了解化合价变化的实质以及化合价的变化与得失电子之间的关系
2、学生在初中化学一年的学习中对化学知识有了初步了解,有一定的搜集和处理信息的能力、获取新知识的能力、分析和解决问题的能力以及交流与合作的能力,但仍有待提高
二、教学目标(一)、知识与技能1、通过分析化学反应中元素化合价的变化,使学生理解氧化还原反应的概念
2、通过化合价的升高或电子的得失,学会判断一个反应中的氧化剂和还原剂
3、通过对典型化学反应的分析,使学生掌握氧化还原反应的本质是电子转移
(二)、过程与方法1、通过对氧化还原反应的学习,学会怎样从特殊到一般规律,再从一般规律到特殊的认识问题的科学方法
2、通过对氧化剂和还原剂这一矛盾体的学习,使学生建立对立统一的观点分析问题的意识
(三)情感态度价值观1、通过氧化还原反应概念的演变,培养学生用发展的眼光、