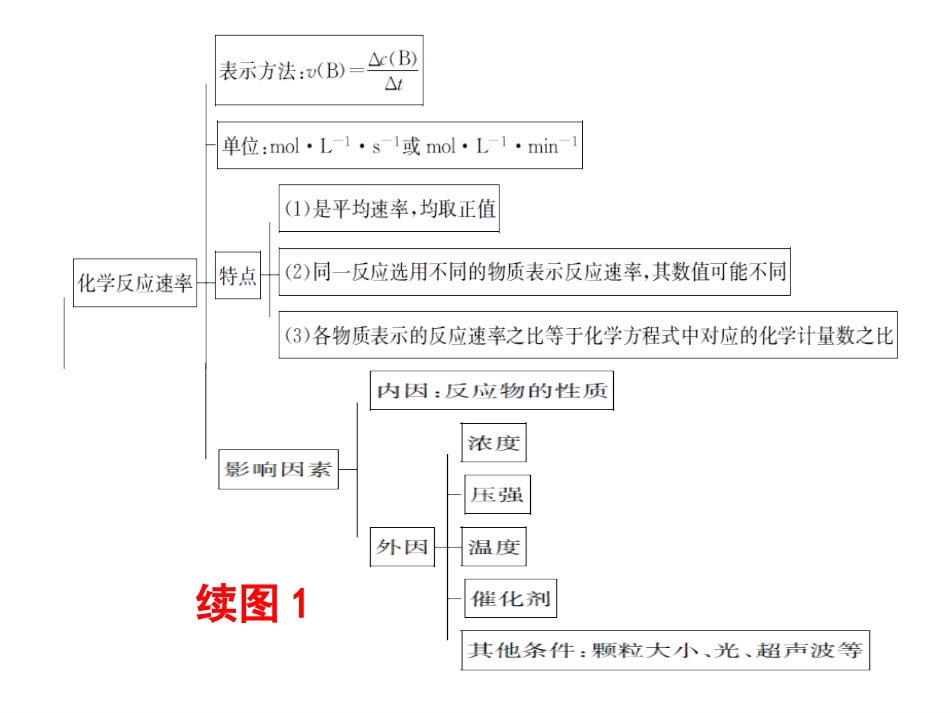
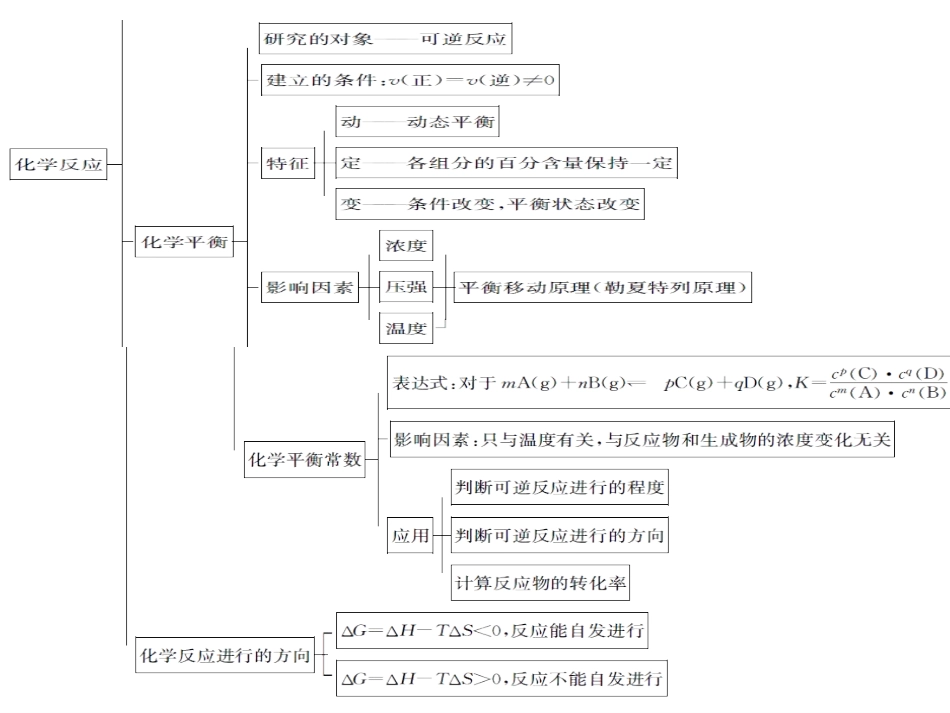
化学化学第二章复习课续图1在2A+B3C+4D反应中,表示该反应速率最快的是()
v(A)=0
5molL•-1s•-1B
v(B)=0
3molL•-1s•-1C
v(C)=0
8molL•-1s•-1D
v(D)=1molL•-1s•-1B某温度下,可逆反应:mA(g)+nB(g)pC(g)的平衡常数为K,下列有关K的说法正确的是()
K值越大,表明该反应越有利于C的生成,反应物的转化率越大B
若缩小反应器的容积,能使平衡正向移动,则K增大C
温度越高,K一定越大D
如果m+n=p,则K=1A化学A
该反应的ΔH0)B
2SO3(g)2SO2(g)+O2(g)ΔH=+Q2kJmol•-1(Q2>0)C
4NH3(g)+5O2(g)4NO(g)+6H2O(g)ΔH=-Q3kJmol•-1(Q3>0)D
H2(g)+CO(g)C(s)+H2O(g)ΔH=+Q4kJmol•-1(Q4>0)化学在容积一定的密闭容器中发生可逆反应:A(g)+2B(g)2C(g)ΔH=+Q(Q>0),条件变化时,影响平衡移动的关系如图所示
下列说法不正确的是()
p1>p2,纵坐标可能是B的转化率B
p1>p2,纵坐标可能是C的质量分数C
p1p2,纵坐标可能是A的转化率C化学在密闭容器中,给一氧化碳和水蒸气的混合气体加热,在催化剂存在下发生反应:CO(g)+H2O(g)H2(g)+CO2(g)
在500℃时,平衡常数K=9
若反应开始时,一氧化碳和水蒸气的浓度都是0
02molL•-1,则在此条件下CO的转化率为()
80%C密闭容器中发生如下反应:A(g)+3B(g)2C(g)ΔH”“0
16molL•-1min•-1