第1讲化学能与热能知识梳理·题型构建考点一I焓变与反应热(3)化学反应中的能量转化形式:、光能、电能等
通常主要表现为的变化
1.化学反应中的能量变化(1)化学反应中的两大变化:变化和变化
(2)化学反应中的两大守恒:守恒和守恒
2.焓变、反应热在条件下进行的反应的
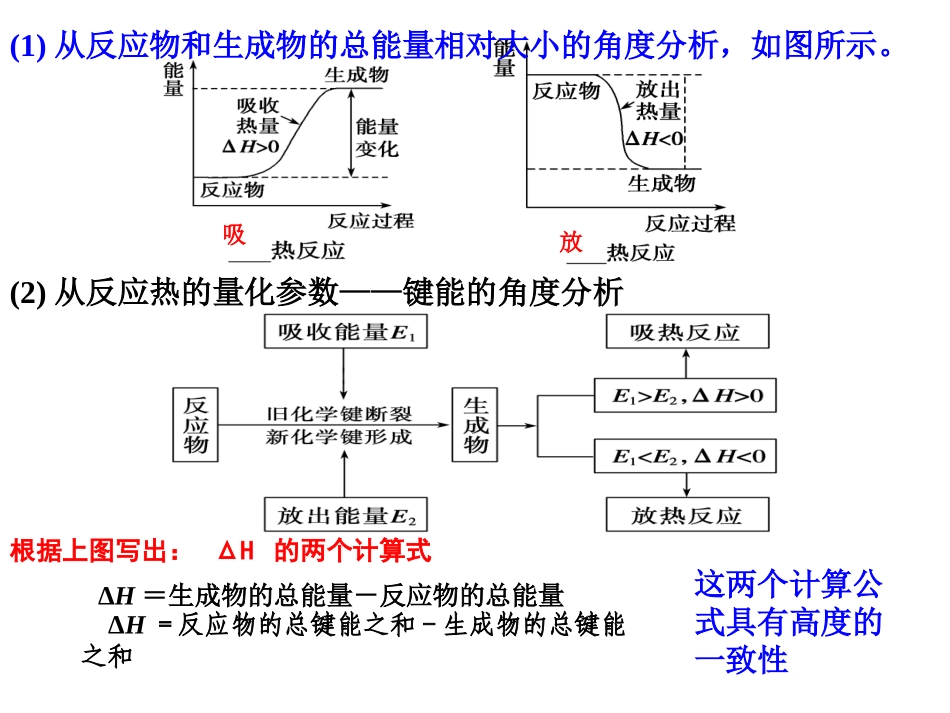
(1)定义:(2)符号:(3)单位:3.吸热反应和放热反应物质能量质量能量热能热量恒压热效应ΔH:放热“—”,吸热“+”kJ·mol-1kJ/mol(1)从反应物和生成物的总能量相对大小的角度分析,如图所示
任何化学反应一定伴随着能量的变化知识梳理·题型构建(2)从反应热的量化参数——键能的角度分析吸放(1)从反应物和生成物的总能量相对大小的角度分析,如图所示
根据上图写出:ΔH的两个计算式ΔH=反应物的总键能之和-生成物的总键能之和ΔH=生成物的总能量-反应物的总能量这两个计算公式具有高度的一致性①大多数分解反应;②盐的水解和弱电解质的电离;③Ba(OH)2·8H2O与NH4Cl反应;④碳和水蒸气、C和CO2的反应
(3)常见放热反应①可燃物的燃烧;②酸碱中和反应;③大多数化合反应;④金属跟酸的置换反应;⑤物质的缓慢氧化
(4)常见吸热反应1.同质量的硫粉在空气中燃烧和在纯氧中燃烧,哪一个放出的热量多,为什么
答案在空气中燃烧放出的热量多,因在纯氧中燃烧火焰明亮,转化成的光能多,故放出的热量少
2.判断正误,正确的划“√”,错误的划“×”(1)放热反应不需要加热就能反应,吸热反应不加热就不能反应()(2)物质发生化学变化都伴有能量的变化()(3)伴有能量变化的物质变化都是化学变化()(4)吸热反应在任何条件都不能发生()(5)Na转化为Na+时,吸收的能量就是该过程的反应热()(6)水蒸气变为液态水时放出的能量就是该变化的反应热()深度思考深度思考知识梳理·题型构建×√××××知识梳理·题型构建1.某反