实验三:演示实验的准备与实验教学研究 ——氧气的获得方法及氧气的性质 一、 实验计划 (1 )实验内容 1、 了解实验室制备气体有哪几种制气装置,制取各类气体适合的仪器装置、收集方法及尾气的吸收; 2、 熟悉实验室制取氧气的几种方法,并能按绿色化学的理念判断、选择合适的实验室获得氧气的方法; 3、 探讨氧气性质实验鲜明、生动、直观的方法及仪器装置,熟练掌握每一个氧气性质实验的操作技能和成败关键; 4、 学习和研究氧气性质实验的教学技能; 5、 体验教师课前做好预备实验的重要性,培养良好的实验教学态度和习惯
(2 )实验计划 ①获得氧气的方法: 2KClO32KCl+3O2↑ 2KMnO4K2MnO4+MnO2+O2↑ 2H2O22H2O+O2↑(催化剂 MnO2) a、氯酸钾(KClO3)在二氧化锰(MnO2 )做催化剂的条件下,加热制备氧气
注意氯酸钾与二氧化锰二者的比例关系应为 6:1较为恰当,若二氧化锰的量过多,则有副反应,导致有氯气(Cl2)产生
实验装置如图 7-4所示
注意装置中,试管口不要塞棉花,因为氯酸钾(KClO3)是易燃物,在长时间的加热的条件下,可能会发生危险
收集氧气时可用向上排空气法或用排水法
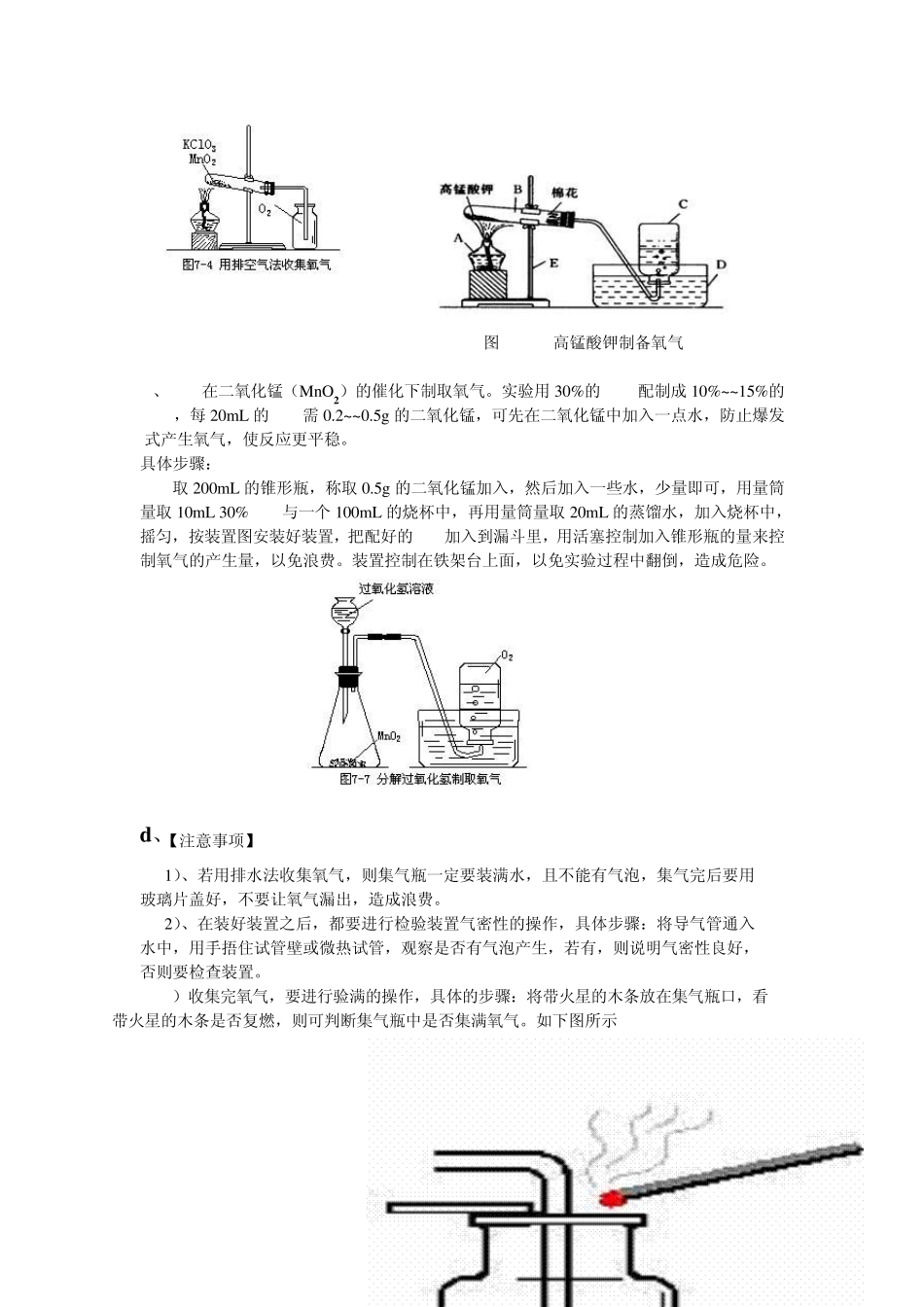
b、高锰酸钾(KMnO4)加热制备氧气
实验装置如图 7-5所示
注意装置中,试管口要塞棉花,因为高锰酸钾是紫红色固体,加热时会有紫红色蒸汽产生,若没有塞棉花,会影响氧气的纯度,使制备的氧气略带紫红色
收集氧气时可用向上排空气法或排水法
MnO2 图7-5 高锰酸钾制备氧气 c、H2O2 在二氧化锰(MnO2)的催化下制取氧气
实验用 30%的 H2O2 配制成 10%~~15%的H2O2 ,每 20mL 的 H2O2 需 0
5g 的二氧化锰,可先在二氧化锰中加入一点水,防止爆发式产生氧气,使反应更平稳
具体步骤: 取 200mL 的锥形