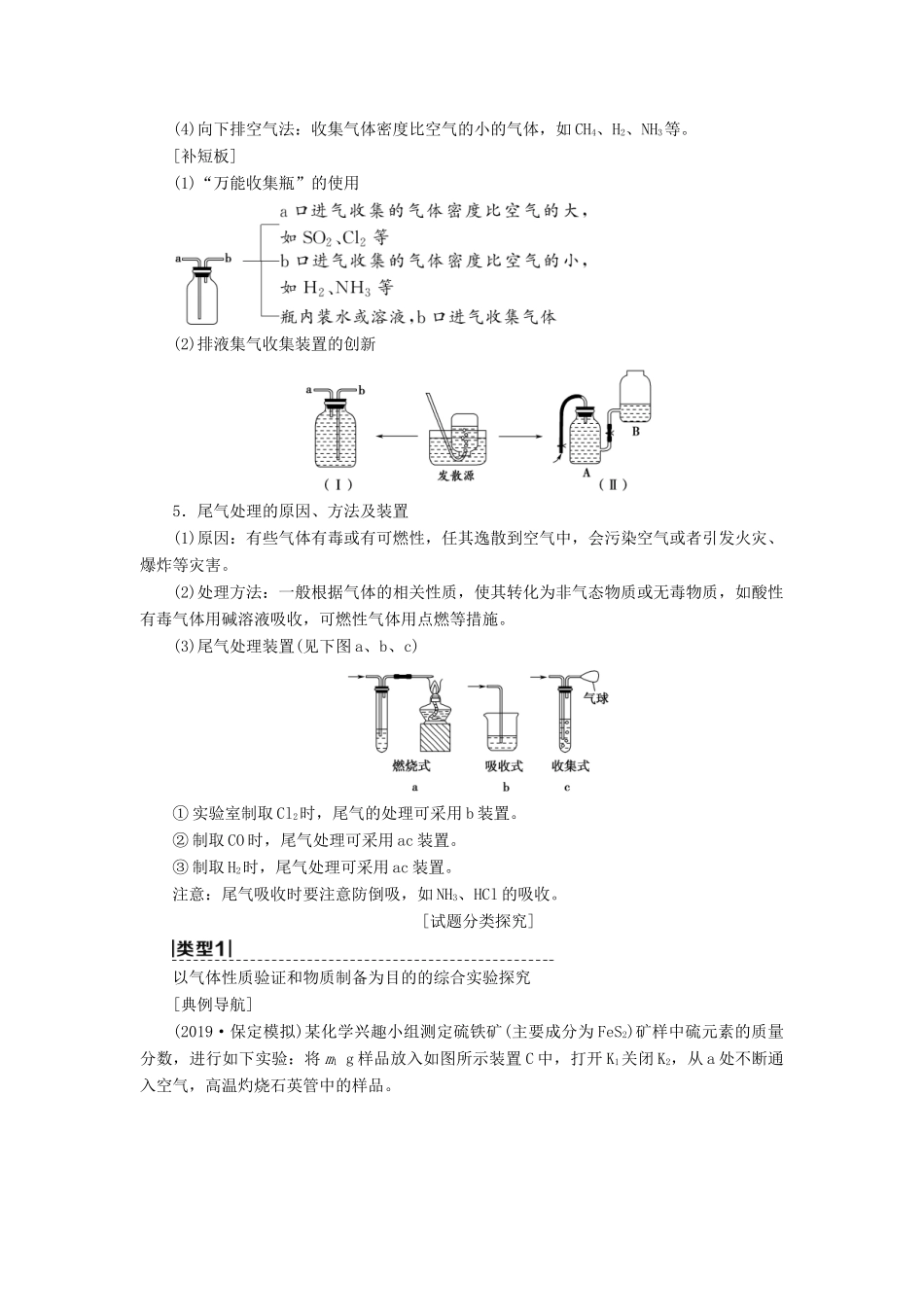
第 4 章 非金属及其化合物(二) 常见气体的实验室制法及其性质探究[核心整合归纳]1.气体制备及其性质探究的基本思路2.常见气体的发生装置 反应装置类型反应装置图适用气体操作注意事项固、固加热型O2、NH3等① 试管要干燥;② 试管口略低于试管底;③ 加热时先均匀加热再固定加强热固、液加热型或液、液加热型Cl2、HCl 等① 烧瓶加热时要隔石棉网;② 反应物均为液体时,烧瓶内要加碎瓷片(或沸石)固、液不加热型或液、液不加热型H2、CO2、SO2、NO、NO2等① 使用长颈漏斗时,要使漏斗下端插入液面以下;② 启普发生器只适用于块状固体和液体反应,且气体不溶于水;③ 使用分液漏斗既可以增强气密性,又可控制液体流速[补短板]“固+液――→气”装置的改进(1)控制温度(图 1)(2)平衡气压、便于液体滴下(图 2) 图 1 图 23.常见气体的净化(1)除杂试剂选择的依据:主体气体和杂质气体性质上的差异,如溶解性、酸碱性、氧化性、还原性
除杂原则:①不损失主体气体;②不引入新的杂质气体;③在密闭装置内进行;④先除易除的杂质气体
(2)气体干燥净化装置类型液态干燥剂固态干燥剂固态干燥剂固体,加热装置ⅠⅡⅢⅣ常见干燥剂浓硫酸(酸性、强氧化性)无水氯化钙(中性)碱石灰(碱性)除杂试剂Cu、CuO、Mg 等[补短板](1)需净化的气体中含有多种杂质时,除杂顺序:一般先除去酸性气体,如氯化氢气体、CO2、SO2等,水蒸气要在最后除去
(2)选用除杂方法时要保证杂质完全除掉,如除 CO2最好用 NaOH 不用 Ca(OH)2溶液
有时候为了保证气体除尽,还要验证一步,如验证混合气体中既有 CO2,又有 SO2,通常用品红溶液检验 SO2,然后用溴水或酸性 KMnO4溶液除去 SO2,再用品红溶液检验是否除尽,最后用澄清石灰水检验 CO2
(3)酸性干燥(浓硫酸、P2O5):不能干燥 NH3