3 氧化还原反应1
了解氧化还原反应的本质是电子转移;2
能正确理解氧化还原反应的概念及概念间的相互关系;3
能用单、双线桥正确表示氧化还原反应中电子转移的方向和数目;4
能正确判断氧化剂、还原剂、氧化产物、还原产物
掌握氧化还原反应方程式的配平方法和技巧;6
灵活运用电子转移守恒法进行氧化还原反应的相关计算
一、氧化还原反应的相关概念 1.本质和特征2.有关概念及其相互关系例如:反应 4HCl(浓)+MnO2=====MnCl2+Cl2↑+2H2O 中,氧化剂是 MnO2,氧化产物是 Cl2,还原剂是 HCl,还原产物是 MnCl2;生成 1 mol Cl2时转移电子的物质的量为 2_mol,被氧化的 HCl 的物质的量是 2_mol
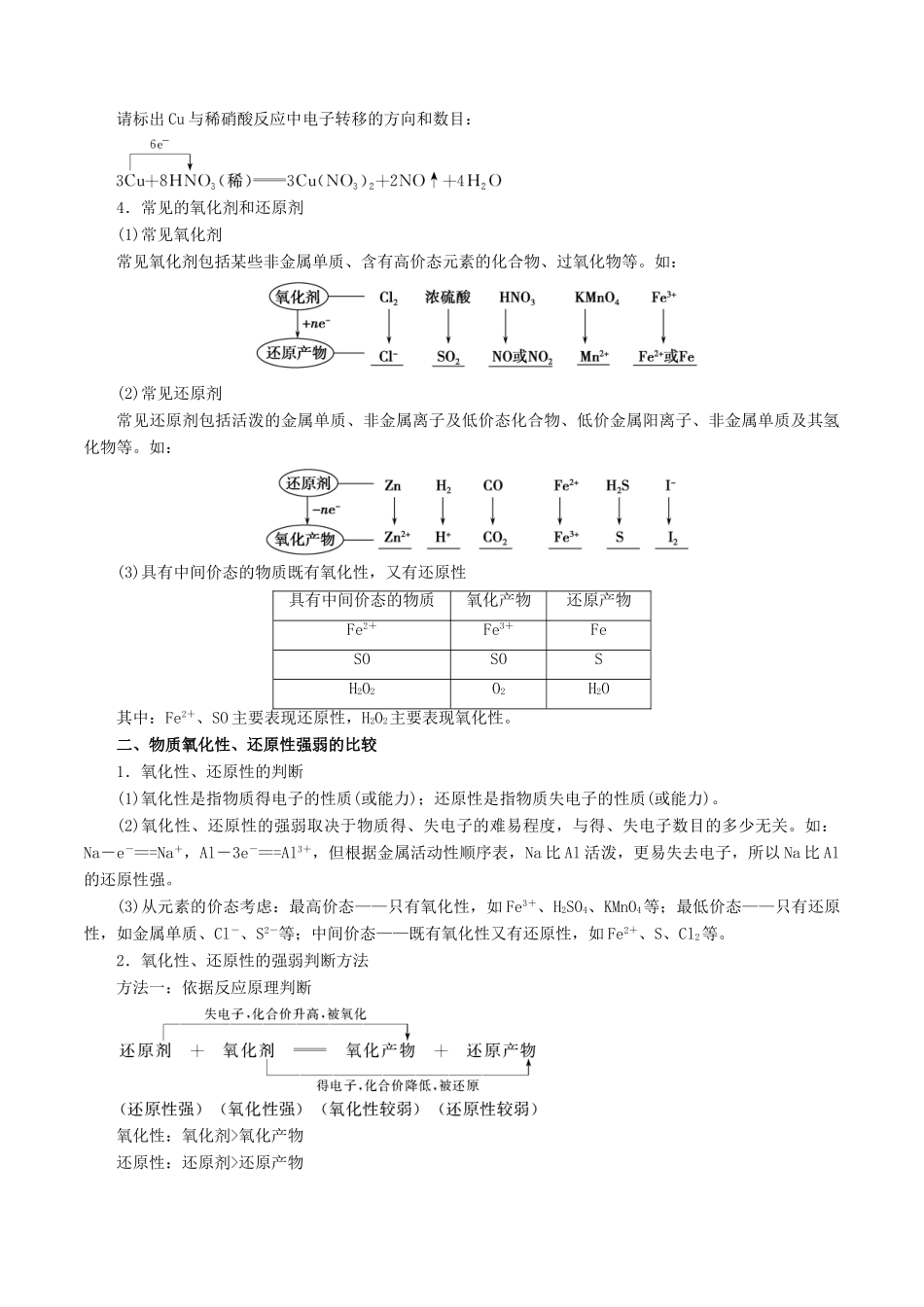
3.氧化还原反应中电子转移的表示方法(1)双线桥法请标出 Cu 与稀硝酸反应中电子转移的方向和数目:(2)单线桥法请标出 Cu 与稀硝酸反应中电子转移的方向和数目:4.常见的氧化剂和还原剂(1)常见氧化剂常见氧化剂包括某些非金属单质、含有高价态元素的化合物、过氧化物等
如:(2)常见还原剂常见还原剂包括活泼的金属单质、非金属离子及低价态化合物、低价金属阳离子、非金属单质及其氢化物等
如:(3)具有中间价态的物质既有氧化性,又有还原性具有中间价态的物质氧化产物还原产物Fe2+Fe3+FeSOSOSH2O2O2H2O其中:Fe2+、SO 主要表现还原性,H2O2主要表现氧化性
二、物质氧化性、还原性强弱的比较 1.氧化性、还原性的判断(1)氧化性是指物质得电子的性质(或能力);还原性是指物质失电子的性质(或能力)
(2)氧化性、还原性的强弱取决于物质得、失电子的难易程度,与得、失电子数目的多少无关
如:Na-e-===Na+,Al-3e-===Al3+,但根据金属活动性顺序表,Na 比 Al 活泼,更易失去电子,所以 Na 比