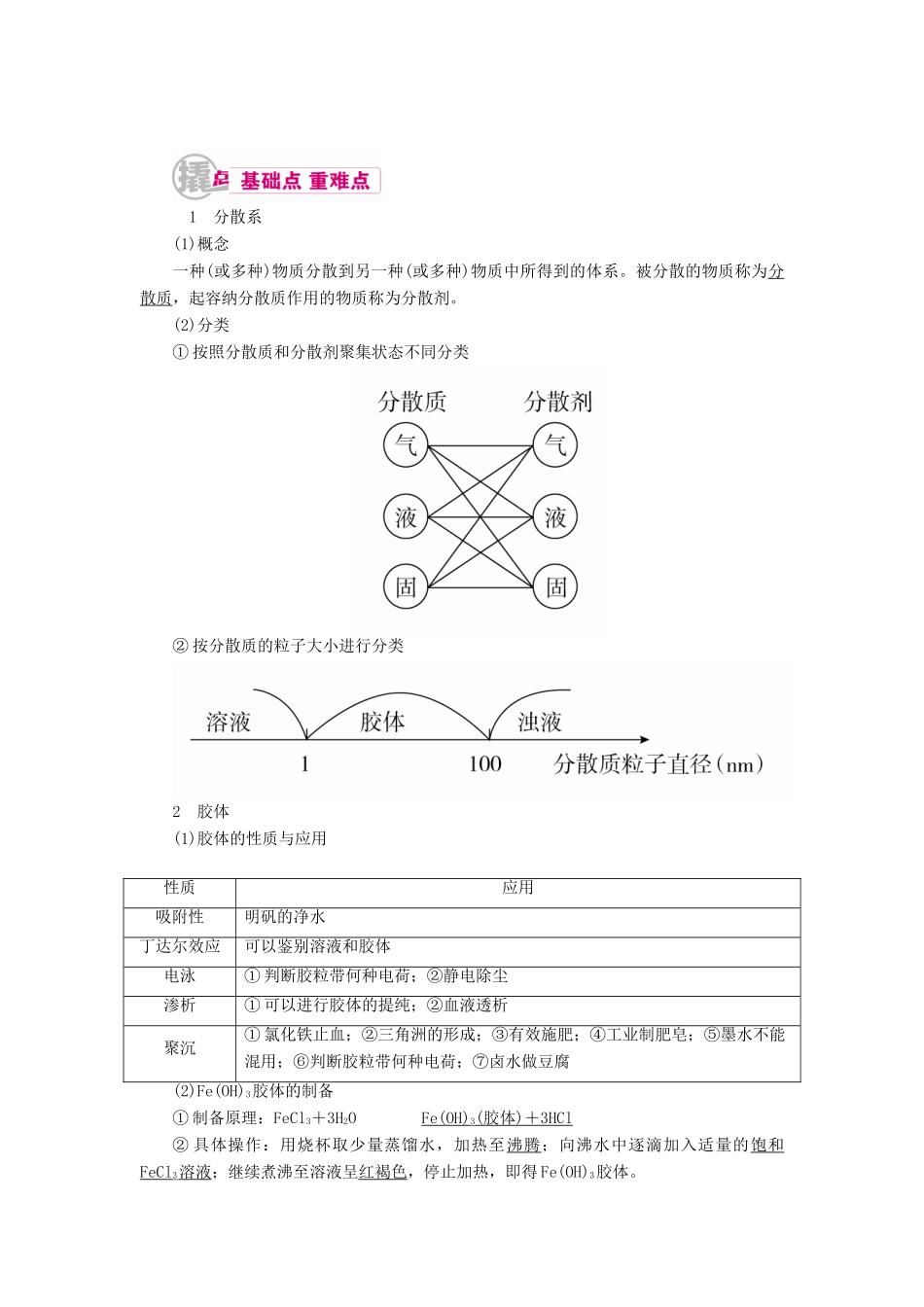
1 分散系(1)概念一种(或多种)物质分散到另一种(或多种)物质中所得到的体系
被分散的物质称为分散质,起容纳分散质作用的物质称为分散剂
(2)分类① 按照分散质和分散剂聚集状态不同分类② 按分散质的粒子大小进行分类2 胶体(1)胶体的性质与应用性质应用吸附性明矾的净水丁达尔效应可以鉴别溶液和胶体电泳① 判断胶粒带何种电荷;②静电除尘渗析① 可以进行胶体的提纯;②血液透析聚沉① 氯化铁止血;②三角洲的形成;③有效施肥;④工业制肥皂;⑤墨水不能混用;⑥判断胶粒带何种电荷;⑦卤水做豆腐(2)Fe(OH)3胶体的制备① 制备原理:FeCl3+3H2OFe(OH)3( 胶体 ) + 3HCl ② 具体操作:用烧杯取少量蒸馏水,加热至沸腾;向沸水中逐滴加入适量的饱和FeCl3 溶液;继续煮沸至溶液呈红褐色,停止加热,即得 Fe(OH)3胶体
学霸巧学卡 正确认识“胶体”(1)胶体与其他分散系的本质区别:胶体粒子的直径在 1~100 nm 之间,这是胶体的本质特征,也是胶体区别于其他分散系的依据,同时也决定了胶体的性质
(2)胶体属于分散系,是混合物,而很多纳米级物质的微粒直径也是在 1~100 nm 之间,但不属于胶体,属于纯净物,如纳米铜等
(3)胶体是电中性的,所谓“胶体带电”实质上是胶粒带电,而整个胶体不显电性
同种胶粒带相同的电荷,所以胶体能比较稳定地存在,如果加入带相反电荷胶粒的胶体或电解质溶液,胶体就会发生聚沉
(4)区分胶体和溶液的最简单方法为丁达尔效应,分离胶体和溶液的操作是渗析
丁达尔效应与渗析都是物理变化,不是化学变化
(5)胶体微粒一般是离子、分子或难溶物的聚集体,但有些高分子化合物,如淀粉、蛋白质,因其分子非常大,其相对分子质量通常为几万、几十万甚至上百万、千万,因此一个分子就是一个胶体微粒,它们的溶液是胶体
(6)氢氧化铁胶体中的胶粒不是指 1 个